(本题共12分)
我国利用生产磷铵[(NH4)3PO4]排放的废渣磷灰石制取硫酸并联产水泥的技术研究获得成功。已知磷灰石的主要成分是Ca3(PO4)2,具体生产磷铵流程如下:
38.操作a的名称是___________,实验室中进行此操作的非玻璃仪器用品有___________;在实验室中操作b的名称是______________________。
39.装置a中生成两种酸式盐,它们的化学式分别是_______________________。
40.固体A中一定含有的物质,其化学式是_________________。
41.热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,气、液热交换时通常使用的仪器是________________________。
42. 制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的试剂是__________。
a.NaOH溶液、酚酞试液 b.KMnO4溶液、稀硫酸
c. 碘水、淀粉溶液 d.氨水、酚酞试液
所用的测量方法为 。
某次实验需配制0.4 mol·L-1NaOH溶液500 mL。配制方法如下:
(1)配制该溶液应选用 mL容量瓶;
(2)用托盘天平准确称量 g固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约200 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待 后,将烧杯中的溶液注入容量瓶中;
(4)用少量 洗涤烧杯以及玻璃棒2~3次,洗涤后的溶液 ,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面 时,改用
加蒸馏水至液面与刻度线相切。盖好瓶塞, 。
(6)误差分析:(填偏高、偏低、无影响)
若容量瓶中洗净后未干燥,残留少量水,则所配制的溶液浓度将;
操作(5)中,若定容时,眼睛俯视,则所配制的溶液浓度将。
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
(一)制备
下图是实验室制备PCI3的装置(部分仪器已省略)
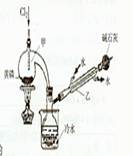
(1)仪器乙的名称;
(2)实验室制备Cl2的离子方程式:;
(3)碱石灰的作用是,;
(4)向仪器甲中通人干燥Cl2之前,应先通人一段时间的CO2,其目的是。
(二)提纯
粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过____(填实验操作名称),即可得到PCl3的纯品。
(三)分析
测定产品中PCl3纯度的方法如下:迅速称取m,g产品,水解完全后配成500mL溶液,取出2 5.00mL加入过量的c1mol·L-lV1mL碘溶液,充分反应后再用c2mol·L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液。
5.00mL加入过量的c1mol·L-lV1mL碘溶液,充分反应后再用c2mol·L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应。
根据上述数据,该产品中PCl3的质量分数为(用含字母的代数式表示、不必化简)
某研究性学习小组通过查阅资料发现,CuSO4溶液与NaOH溶液反应生成的沉淀中除Cu(OH)2外,还有碱 式硫酸铜[化学式可表示为xCuSO4·yCu(OH)2]。为了加以验证,小组成员进行了如下实验:
式硫酸铜[化学式可表示为xCuSO4·yCu(OH)2]。为了加以验证,小组成员进行了如下实验:
①分别配制50mL物质的量浓度均为0.L00mol.L-1CuSO4溶液和NaOH溶液;
②准确量取l0mLCuSO4溶液倒入50mL烧杯中;
③向烧杯中匀速加入0.l00mol.L—NaOH溶液,并每加入1.00mLNaOH溶液用pH计测一次混合溶液的pH;
④当滴人NaOH溶液的体积达到30mL时停止实验,并绘制出向CuSO4溶液中滴加NaOH溶液时pH变化曲线。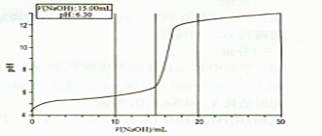
请回答以下问题:
(1)V(NaOH)在0.00mL~2.00mL之间时,溶液中无沉淀产生,但pH变化较快的原因是;
(2)V(NaOH)在2.00mL~ 15.00mL之间时,溶液中产生绿色沉淀,并不断增加,
经检测此沉淀为碱式硫酸铜。已知蒸馏水的pH为6.32,当V(NaOH)为15.00mL时,溶液pH为6.30,则可求得x=,y=;
(3)V(NaOH)在17.00mL~20.00mL之间时,溶液中出现蓝色沉淀,并不断增
加。已知V(NaOH)为20.00mL时,溶液pH为12.25,则此时沉淀中(填
“含”或“不含”)有碱式硫酸铜,理由是。
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实 验方案:
验方案:
方案一:取三块镀锌铁皮(A、B、C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40mL 6mol·L—1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤、小心烘干、称量。将B、C重复上面的实验。
(1)锌镀层完全反应的标志是。
(2)如何检验铁片已经洗净
。
方案二:已知锌与强碱溶液反应的离子方程式为:Zn+2OH—+2H2O=[Zn(OH)4]2—+H2↑。某同学按右图装置设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为mg的镀锌铁皮放入6mol·L—1 NaOH溶液中。回答下列问题: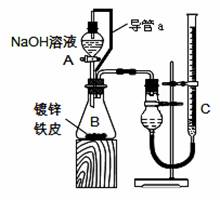
(3)装置中导管a的作用是。
(4)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②待B中不再有气体产生并恢复至室温;③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。
上述操作的顺序是(填序号)。
(5)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL(已知Zn的密度为7.14g/cm3,实验条件的气体摩尔体积为Vm L / mol)。则镀锌铁皮的镀层厚度为cm。(写出数学表达式)
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入__________,目的是__________。
(2)反应中加入过量的乙醇,目的是__________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是
______________________________________________________。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
则试剂a是:____________,分离方法I是____________,分离方法II是____________,
试剂b是___________ ___,分离方法III是______________。
___,分离方法III是______________。
(5)甲、乙两位同学欲将所得含有乙醇、乙酯和水的乙酸乙酯粗产品提纯, 在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
甲得到了显酸性的酯的混合物
乙得到了大量水溶性的物质
丙同学分析了上述实验目标产物后认为上述实验没有成功。
试解答下列问题:
①甲实验失败的原因是:_______________________________________________
②乙实验失败的原因是:_______________________________________________