今有室温下四种溶液,有关叙述正确的是
| |
① |
② |
③ |
④ |
| pH |
11 |
11 |
3 |
3 |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.分别加水稀释10倍,四种溶液的pH ①>②>④>③
B.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
C.①、④两溶液等体积混合,所得溶液中c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb= 9∶11
下图是部分短周期主族元素原子半径与原子序数的关系图。则下列说法正确的是
| A.Y、R两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 |
| B.简单离子的半径:X > Z > M |
| C.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z单质能从M与R元素构成的盐溶液中置换出单质M |
下列实验装置设计正确的是
下列关于有机化合物的说法正确的是
| A.乙醇和乙酸均能与钠反应生成氢气 |
| B.煤的干馏、油脂的皂化和石油的分馏都属于化学变化 |
| C.丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
| D.糖类、油脂、蛋白质均属于高分子化合物 |
化学与社会、生产、生活紧切相关,下列说法正确的是
| A.信息产业中的光缆的主要成份是单质硅 |
| B.NO2、CO2、SO2、PM2.5颗粒都会导致酸雨 |
| C.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
| D.发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 |
电化学降解NO3-的原理如图所示,若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为a克,则a值为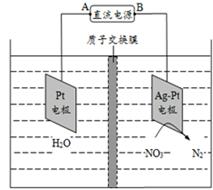
| A.14.4 | B.10.4 | C.12.4 | D.14.0 |