25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是 
| A.W点所示的溶液中:c (Na+)+c (H+)=2c(CO32- )+c (OH-)+c (Cl-) |
| B.pH= 4的溶液中:c (H2CO3)+c (HCO3-)+c (CO32-)<0.1mol·L-1 |
| C.pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3-)= c (OH-)+c (Cl- ) |
| D.pH=11的溶液中:c (Na+)>c (Cl-)>c (CO32- )>c (HCO3- )>c (H2CO3) |
以下除杂试剂或方法错误的是
| 选项 |
物质 |
杂质 |
除杂试剂 |
反应条件或除杂方法 |
| A |
苯 |
乙酸 |
烧碱溶液 |
分液 |
| B |
硅 |
铝 |
稀盐酸 |
过滤 |
| C |
氯气 |
氯化氢 |
饱和食盐水 |
洗气 |
| D |
乙烷 |
乙烯 |
氢气 |
催化剂、加热 |
下列叙述中错误的是
| A.葡萄糖和果糖互为同分异构体 | B.淀粉、油脂、蛋白质均能发生水解反应 |
| C.乙醇可使酸性高锰酸钾溶液褪色 | D.苯和溴水在FeBr3的条件下可制得溴苯 |
下列物质既含有离子键又含有极性键和非极性键的是
| A.KOH | B.H2O2 | C.CH3COONa | D.NH4Cl |
下列实验的实验目的、图示操作和实验现象均正确的是
| A. 探究不同催化剂对同一反应速率的影响 |
B. 探究温度对化学平衡的影响 |
 试剂:淀粉溶液、碘水、 唾液、2mol/L H2SO4溶液 现象:图中左试管溶液颜色一段时间后逐渐变蓝色,右试管溶液颜色迅速变蓝色 |
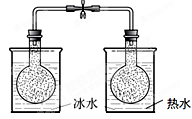 2NO2(g)  N2O4 △H<0 N2O4 △H<0试剂:烧瓶中各充入等质量的NO2 现象:一段时间后,右边烧瓶内气体颜色变浅,左边烧瓶内气体颜色变深 |
| C. 探究醋酸、碳酸、硼酸的酸性强弱 |
D. 验证外加电流的阴极保护法 |
 试剂:0.1 mol/L醋酸溶液、饱和硼酸溶液 0.1 mol/LNa2CO3溶液 现象:图中左试管内液面产生气泡,右试管无明显现象 |
 试剂:酸化的3%的NaCl溶液、 铁氰化钾溶液 现象:一段时间后,向烧杯中滴加2滴铁氰化钾溶液,不产生蓝色沉淀 |
下列现象不能用沉淀溶解平衡移动原理解释的是
| A.相同温度下,AgCl在水中的溶解度大于在氯化钠溶液中的溶解度 |
| B.浓FeCl3溶液滴入沸水加热形成红褐色透明液体 |
| C.自然界地表层原生铜矿变成CuSO4溶液向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS) |
| D.加入少量AgCl固体可以除去氯化钠溶液中的少量硫化钠杂质 |