[化学—选修2化学与技术](15分)
(1)下列关于工业生产说法正确的是 。(填序号)
| A.在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气 |
| B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 |
| C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室 |
| D.工业上采用电解熔融氯化铝的方法制取金属铝 |
E.石油裂化属于化学变化,主要目的是为了获得短链不饱和气态烃
(2)我国规定饮用水质量标准规定必须符合下表中要求:
| pH |
Ca2+ 、Mg2+总浓度 |
细菌总数 |
| 6.5~8.5 |
< 0.004 5 mol·L-1 |
<100个·mL-1 |
以下是原水处理成自来水的工艺流程示意图: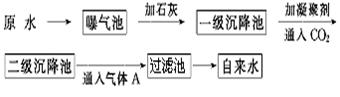
①原水中含Ca2+ 、Mg2+ 、HCO3-、Cl-等,加入石灰生成Ca(OH)2,进而发生若干复分解反应,写出其中的离子方程式(只要求写出两个): ; 。
②FeSO4·7H2O是常用的凝聚剂,它在水中最终生成 沉淀;通入二氧化碳的目的是 和 。
③气体A的作用是 ,通常可以用Ca(ClO)2替代A,下列物质中 同样可以作为气体A的代用品(填编号,多选倒扣)。
a.ClO2 b.浓氨水 c.K2FeO4 d.SO2
【化学与技术】钛铁矿的主要成分可表示为FeTiO3(Ti 为+4 价),某钛铁矿中含FeTiO3 为76%。钛白粉在涂料、塑料、油墨、造纸等行业具有广泛的用途,钛白粉的主要成分为TiO2。利用该钛铁矿生产钛白粉及绿矾的工艺流程如下: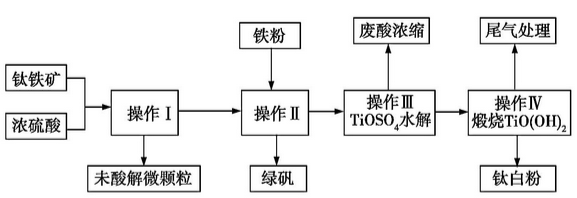
(1)若钛铁矿与浓硫酸反应时Ti 的转化率为92%,操作Ⅰ~Ⅳ中Ti 的转化率均为96%,则1t 该矿石可生产钛白粉(TiO2) t (计算结果保留两位小数,下同),能否计算生成的绿矾(FeSO4·7H2O)的质量? (能则写出计算结果,不能则说明理由)。
(2)钛铁矿与硫酸的反应可表示为FeTiO3+H2SO4 →TiOSO4+X+H2O(未配平)。其中X的化学式为 。
(3)操作Ⅰ的名称是 ,操作Ⅱ包括冷却结晶、 。操作Ⅱ中加入铁粉的目的是 (用离子方程式表示)。
(4)写出操作Ⅲ中TiOSO4水解的化学方程式: 。
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。如图是以铁屑为原料制备K2FeO4的工艺流程图:
请回答下列问题:
(1)氯气与铁屑反应生成FeCl3的条件是 ,其生成物氯化铁也可作净水剂,其净水原理为 。
(2)流程图中的吸收剂X 为 (选填字母代号)。
a.NaOH 溶液 b.Fe 粉
c.FeSO4溶液 d.FeCl2溶液
(3)氯气与NaOH 溶液反应生成氧化剂Y 的离子方程式为 。
(4)反应④的化学方程式为 ,该反应中氧化剂与还原剂的物质的量之比为 。
(5)K2FeO4的净水原理是 ,该反应生成具有吸附性的Fe(OH)3。用上述方法制备的粗K2FeO4需要提纯,可采用重结晶、洗涤、低温烘干的方法,洗涤剂可选用稀KOH 溶液,原因是 。
,该反应生成具有吸附性的Fe(OH)3。用上述方法制备的粗K2FeO4需要提纯,可采用重结晶、洗涤、低温烘干的方法,洗涤剂可选用稀KOH 溶液,原因是 。
(6)测定制备的粗K2FeO4的纯度可用滴定法,滴定时有关反应的离子方程式为:
现称取1.98 g 粗K2FeO4样品溶于适量KOH 溶液中,加入稍过量的KCrO2,充分反应后过滤,滤液在250 mL 容量瓶中定容。每次取25.00 mL 加入稀硫酸酸化,用0.100 0 mol·L-1的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中K2FeO4的质量分数为 。
粗锡的主要成分是锡,另外含有锌、铜、银、金等杂质。如图甲是工业上用电解法提
纯粗锡的一种工艺流程,电解装置如图乙所示。
(1)流程图中的硅氟酸(化学式为H2SiF6)是一种强酸,其中Si 的化合价为 ,其电离方程式为 。
(2)硅氟酸有腐蚀性,能与SiO2反应。电解粗锡可选取的电解槽有 (选填字母代号)。
a.玻璃电解槽b.石英电解槽
c.塑料电解槽 d.蜡制电解槽
(3)粗锡为电极 (选填“a”或“b”),该电极为 (选填“阳极”或“阴极”),电极反应式为 。
(4)阳极泥中含有的主要物质为 (写化学式)。
(5)若电解时采用SnCl2溶液作为电解液,当阴极增重11.90 g 时,电解质溶液减少的质量为0.54 g,则粗锡减少的质量为 (结果保留两位小数,不考虑进入阳极泥的物质)。
一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
(1)原NaOH溶液的质量分数为________________。
(2)所得溶液中Cl-的物质的量为______________mol。
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2)∶n(H2)=________________。
工业上电解饱和食盐水前,需要对食盐进行精制。已知工业食盐中含有Ca2+、Mg2+、SO42-等杂质。现欲把工业食盐精炼成精盐,请回答下列问题:
(1)欲除去SO42-必须加入可溶性的钡试剂,该试剂不可以是____________________。你选该试剂的理由是______________________。(共2分)
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)若选用的试剂是BaCl2、NaOH、Na2CO3和HCl,下列加入试剂的顺序不合理的是____________。
A.BaCl2、NaOH、Na2CO3、HCl
B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、NaOH、BaCl2、HCl
(3)在选用不同的试剂和不同的加试剂顺序时,都是最后加入盐酸。你认为加入盐酸的作用是(离子方程式表示_________________;__________________。(共4分)