氯气和氯乙烯都是重要的化工产品,年产量均在107t左右。氯气的实验室制备和氯乙烯的工业生产都有多种不同方法。
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要
(2)实验室用2.00mol/L的盐酸和漂粉精[成分为、]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为
(3)实验室通常用向上排空气法收集氯气。设计一个简单实验,验证所收集的氯气中是否含有空气。
4)工业上用电石-乙炔法生产乙烯的反应如下:
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。
电石-乙炔法的缺点是
(5)乙烷和氯气反应可制得,加热分解得到氯乙烯和氯化氢。设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件)。
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。
实验室用固体NaOH配制0.5 mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯②100 mL量筒 ③500mL容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码)
(1)配制时,不需要使用的仪器和用品有____________(填序号),还缺少的仪器是 。
(2)下列操作会使配制的溶液浓度偏低的是 (填字母)
A.没有将洗涤液转移到容量瓶B.转移过程中有少量溶液溅出
C.容量瓶洗净后未干燥 D.定容时俯视刻度线
(3)在容量瓶使用方法中,下列操作不正确的是(填序号)
A.容量瓶用蒸馏水洗净后,再用碱液润洗
B.使用容量瓶前检查它是否漏水
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(4)下列实验操作步骤的正确顺序是(填序号,不能重复) ;
①用托盘天平称量10g NaOH固体放入小烧杯中,加适量蒸馏水溶解;
②继续向容量瓶中加蒸馏水至液面距刻度线1-2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面的最低处与刻度线相切;
③把恢复室温的溶液小心地转入500mL容量瓶中;
④将容量瓶塞紧,充分摇匀;
⑤用少量蒸馏水洗涤烧杯与玻璃棒2-3次,洗涤液一并转移到容量瓶中。
(5)实验中还需要2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取NaOH的质量分别是 (填序号)
A.1000mL,80g B.950mL,76g C.任意规格,72gD.500mL,42g
按如图所示装置进行铁和水蒸气反应的实验。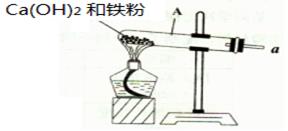
已知:铁与水蒸气反应生成产物有磁性氧化物及可燃性气体。
(1)写出试管A中发生反应的化学方程: ,
(2)为检验铁与水蒸气反应生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)a- ,描述能证明气体产物的实验现象 ;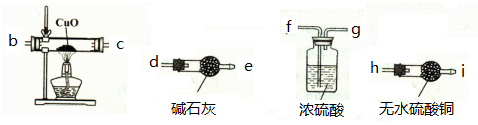
(3)待试管A冷却后,取少量其中的固体物质进行如下实验: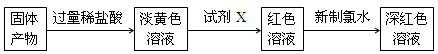
①试剂X的化学式 ;
②用离子方程式表示加入新制氯水后溶液红色加深的原因 ;
③若在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色的原因进行探究。
I.提出假设:
假设1:溶液中的SCN-被氧化;
假设2:溶液中的Fe3+被氧化;
假设3: 。
II.设计方案:请对所提出的假设2进行验证,写出实验方案。
III.方案实施(略)。
某化学兴趣小组进行草酸亚铁晶体(FeC2O4·nH2O)分解的实验探究。
经过小组讨论,他们设计了如下装置进行实验(夹持装置未画出):烧瓶A中盛有饱和NH4Cl和饱和NaNO2混合液(常用于实验室制取N2),干燥管B、G中均装有碱石灰,试管D、F、I中盛有澄清石灰水。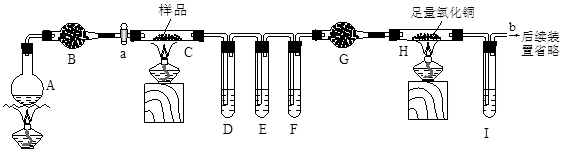
(1)连接好装置后,加入药品前应该进行的实验操作是_____________(填操作名称)。
(2)实验时先打开活塞a,并加热烧瓶A一段时间,其目的是___________________。
(3)试管E中的试剂为:________________。
(4)装置F的作用:______ ___。
Ⅰ.定性研究
(5)试管D中出现浑浊,证明产物中有____________存在;证明分解产物中存在CO的现象是_________________;要证明分解时产生的另一种气态产物的存在应该如何改进装置_____________;装置C反应后的固体残余物(经测无Fe),在煮沸的稀硫酸中完全溶解,取反应液加入KSCN溶液无血红色,证明固体产物为____________。
Ⅱ.定量分析(假定每一步反应进行完全)
(6)取7.2 g样品进行上述实验,测得硬质玻璃管C中残余固体2.88 g,硬质玻璃管H中固体质量减轻0.64 g,则草酸亚铁晶体(FeC2O4·nH2O)分解的化学方程式为__________________。
某校化学课外小组用硫酸铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验。制备硫酸亚铁晶体主要的操作流程如下:
请根据题目要求回答下列问题:
(1)A的化学式为 。
(2)趁热过滤的目的是 。
(3)结晶操作过程中应控制滤液酸性的原因是 。
(4)实验室利用硫酸亚铁铵溶液[(NH4)2Fe(SO4)2]和草酸溶液反应生成草酸亚铁,草酸亚铁晶体(相对分子质量180)受热易分解,某课外小组设计如图的实验装置来检验其分解产物。
①该装置中最不合理的部分 (填字母),原因是 。
②改用正确装置开始实验,B处变蓝,说明草酸亚铁晶体中有 ;C处有白色沉淀,E处黑色粉末变为红色,说明草酸亚铁分解产生 (填化学式)。
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H2SO4(浓)+NaBr  NaHSO4+HBr↑,CH3CH2OH+HBr
NaHSO4+HBr↑,CH3CH2OH+HBr CH3CH2Br+H2O。有关数据见下表:
CH3CH2Br+H2O。有关数据见下表:
| 乙醇 |
溴乙烷 |
溴 |
|
| 状态 |
无色液体 |
无色液体 |
深红色液体 |
| 密度/(g·cm-3) |
0.79 |
1.44 |
3.1 |
| 沸点/℃ |
78.5 |
38.4 |
59 |

(1)A装置的名称是 。
(2)实验中用滴液漏斗代替分液漏斗的优点为 。
(3)给A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,写出此反应的化学方程式 。
(4)给A加热的目的是 ,F接橡皮管导入稀NaOH溶液,其目的主要是 。
(5)图中C中的导管E的末端须在水面以下,其目的是 。
(6)为了除去产品中的主要杂质,最好选择下列__(选填序号)溶液来洗涤所得粗产品
A.氢氧化钠 B.碘化钾 C.亚硫酸钠 D.碳酸氢钠
(7)粗产品用上述溶液洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0 g。
①在上述提纯过程中每次分液时产品均从分液漏斗的_____________(上口或下口)取得。
②从乙醇的角度考虑,本实验所得溴乙烷的产率是______________。