某小组以、、、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体。为测定其组成,进行如下实验。
①氨的测定:精确称取,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%溶液,通入水蒸气,将样品液中的氨全部蒸出,用的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用标准溶液滴定过剩的,到终点时消耗溶液。

②氯的测定:准确称取样品,配成溶液后用标准溶液滴定,溶液为指示剂,至出现淡红色沉淀不再消失为终点(为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是。
(2)用标准溶液滴定过剩的时,应使用式滴定管,可使用的指示剂为。
(3)样品中氨的质量分数表达式为。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将(填"偏高"或"偏低")。
(5)测定氯的过程中,使用棕色滴定管的原因是;滴定终点时,若溶液中=2.0×10-5 ,为。(已知:=1.12×10-12)
(6)经测定,样品中钴.氨.氯的物质的量之比为1:6:3,钴的化合价为,制备的化学方程式为;的制备过程中温度不能过高的原因是。
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。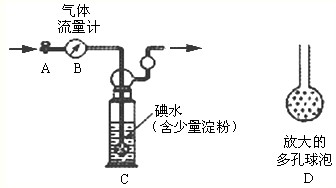
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种:。
(3)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”、“偏低” 或“无影响”)。
乙方案:实验步骤如下面流程图所示:
(4)写出步骤②中反应的化学方程式。
(5)步骤③中洗涤沉淀的方法是。
(6)通过的尾气体积为VL已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为
(用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液中,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由:。
为了测定足量铜与适量一定浓度的浓硝酸反应生成一氧化氮气体和二氧化氮气体的物质的量之比(用m表示),请从下图中选用合适的实验装置,设计一个合理而简单的实验,用于测定m的值。(不考虑二氧化氮转化为四氧化二氮)其中E装置为量气管,由甲、乙两根玻璃管组成,用橡皮管连通,并装入适量水,甲管有刻度(0~50mL),供量气用,乙管可上下移动,用来调节液面高低。回答下列问题: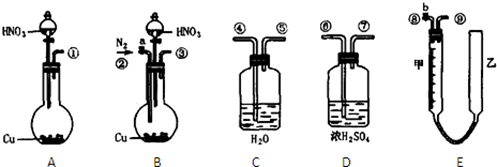
(1)装置的连接顺序是。(填各接口的编号)。
(2)连接好装置并检查气密性后,应打开通入氮气;然后打开____,从乙管注水至充满甲、乙两管,关上a、b。通入氮气的原因是。
(3)实验后,若量气管中气体的体积为VmL(已换算成标准状况下),要测定m的值,还要将___中的溶液做________实验,假设测得其中溶质物质的量为n,用含V和n的式子表示:m=(答案要求化简)。
(4)下列操作中能造成m值偏小的是_。
| A.反应前E中甲管所装水里气泡没赶尽,而最后读数时气泡消失 |
| B.实验后未冷却至室温即开始读数 |
| C.实验前没有先通入足量的氮气 |
| D.实验过程中,E装置乙管的水溢出 |
某学生欲配制6.0 mol/L的H2SO4 1000mL,实验室有三种不同浓度的硫酸:①480 mL 0.5 mol/L的硫酸:②150 mL 25%的硫酸(p=" 1.18" g/mL);③足量的18 mol/L的硫酸。有三种规格的容量瓶:250 mL、500 mL、1000 mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A将①②两溶液全部在烧杯中混合均匀:
B用量筒准确量取所需的18 mol/L的浓硫酸____mL,沿烧杯内壁倒入上述混合液中,并用玻璃棒搅拌,使其混合均匀:
C将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中:
D;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1 cm~2 cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?(填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意。
银氨溶液可用于检测CO气体,实验室研究的装置如图:
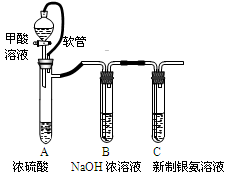 |
已知:银氨溶液制备反应为 Ag++2NH3·H2O=[Ag(NH3)2]++2H2O。 反应结束后试管C底部有黑色沉淀生成,分离出上层清液和底部黑色固体备用。 |
(1)甲酸(HCOOH)遇浓硫酸分解生成CO和H2O,该反应体现浓硫酸的(填“强氧化性”或“脱水性”)。
(2)装置A中软管的作用是。
(3)为验证上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
①实验c的目的是。
②根据上述实验现象判断,上层清液中产物成分为(填化学符号)。
(4)设计实验证明黑色固体的成分是Ag:
可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液。
取少量上述黑色固体,用蒸馏水洗净,,说明黑色固体是Ag单质。(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①写出生成AgCl沉淀的离子反应。
②若该反应中消耗6.6 g羟氨,理论上可得银的质量为g。
现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度,实验时将样品放置于D中。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)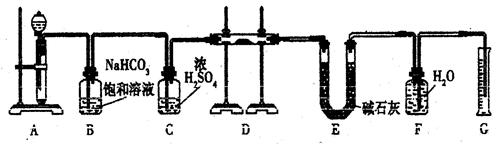
回答下列问题:
(1)装置A中液体试剂选用。
(2)装置B的作用是__ 。
装置C的作用是。
装置E中碱石灰的作用是。
(3)装置D中发生反应的化学方程式是__ 、 ____。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为