同学们在学习Ca(OH)2的化学性质时,对Ca(OH)2溶液和Na2CO3溶液反应后溶液中溶质的成分进行探究。请你一同探究并回答下列问题:
【提出问题】:滤液中的溶质是什么物质?溶液呈中性。
【查阅资料】:①Ca(NO3)2溶液呈中性。 ②Ca(NO3)2 +Na2CO3= CaCO3↓+2NaNO3
【猜想假设】:甲同学认为:只含有NaOH; 乙同学认为:只含有NaOH Ca(OH)2;
丙同学认为:含有NaOH Ca(OH)2 Na2CO3; 你认为可能含有 。
【分析讨论】:丁同学认为 同学的猜想肯定是不合理的,理由是 。
【实验设计】:请你设计一个简单的实验来验证你的猜想是正确的。
| 实验步骤 |
实验现象 |
实验结论 |
| 取滤液于试管中 |
|
猜想正确 |
甲同学也针对自己的猜想进行了如下实验。
| 实验步骤 |
实验现象 |
实验结论 |
| 取滤液于试管中滴加少量的稀盐酸 |
无明显现象 |
猜想正确 |
你认为甲同学的实验结论是否正确 (填正确或不正确),理由是 。
【反思拓展】:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑
。
生活中离不开水。若水的硬度过大,会影响人体健康,因此需要进行软化处理。
(1)小文利用阳离子交换树脂对某硬水水样进行软化,其原理示意如右图所示。树脂的作用是除去硬水中的。
(2)生活中通过煮沸能够降低水的硬度。小文取此水样煮沸后,发现有水垢生成。为探究水垢的成分,他进行了以下实验:
【实验过程】
| 实验序号 |
实验操作 |
实验现象 |
| Ⅰ |
 |
水垢变白、变疏松, 澄清石灰水变浑浊 |
| Ⅱ |
 |
固体部分溶解, 放出热量, 滤液的pH约为12 |
| Ⅲ |
 |
实验现象是。 |
【实验分析及结论】
①由实验Ⅰ可知,水垢分解的产物中一定有。
②实验Ⅲ小试管内发生反应的化学方程式为。
③根据实验探究,推测此水垢的成分中可能含有。
(3)小文另取该水样,加入澄清石灰水,溶液变浑浊,其反应为:
A + Ca(OH)2 ="=" 2CaCO3↓ + 2H2O,则A的化学式为。
某化学小组同学利用以下三组装置探究燃烧条件。
图1图2图3
(1)如图1所示,能燃烧的物质是(填字母序号),燃烧反应的化学方程式为。
A.水中的白磷 B.铜片上的白磷C.铜片上的红磷
(2)如图2所示,将液体a滴入瓶中并与固体b接触,能观察到白磷燃烧,则瓶内发生反应的化学方程式为。
(3)如图3所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。通过上述实验的对比分析,写出产生现象②的原因。
完成三组实验之后,同学成功探究出了燃烧所需要的条件。
为探究四瓶未知无色溶液的成分,甲、乙、丙三组同学分别设计了如下实验。已知四种溶液分别是Na2CO3、NaOH、Ca(OH)2和稀盐酸中的一种。
【实验过程】
甲组实验方案:将四瓶溶液标号分别为1、2、3、4,只利用紫色石蕊溶液进行实验。
| 实验步骤和操作 |
实验现象和结论 |
||
(1)如图所示: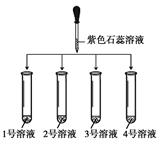 |
① 2号溶液由无色变为红色, 则2号溶液是 ② 另三支试管中溶液均由无色变蓝色 |
||
(2)另取1、3、4号溶液,分别滴加2号溶液
|
① 3号溶液中有气泡放出, 则3号溶液是 ② 另外二支试管中溶液无明显变化 |
||
| (3)另取1、4号溶液,分别滴加 |
①1号溶液中有白色沉淀析出, 则反应的化学方程式为 ② 另一支试管中溶液中无明显变化 |
乙组实验方案:不用其他试剂进行实验。
| 实验操作 |
实验现象 |
实验结论 |
任取三种溶液于三支试管中,分别滴加第四种溶液 |
①一支试管中有气泡放出 其余二支试管中溶液无明显变化 |
① 第四种溶液为稀盐酸 |
| ② 一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
② 第四种为Na2CO3溶液 |
|
| ③ 三支试管中溶液均无明显变化 |
③ 第四种为NaOH溶液 |
【实验分析】
经过交流后,发现实验结论 (填序号)是不正确的;若该结论作正确,对应的实验现象应是 。
丙组实验方案:将四种溶液编号为1、2、3、4,不用其他试剂进行实验。
| 实验操作 |
实验现象 |
实验结论 |
||
如图所示:
|
①A、B、C均无明显变化 ②D中有沉淀析出 |
标号为1、2、3、4的溶液依次为(用化学式表示): 或 |
某化学小组对“SO2能否与H2O反应生成酸”的课题开展探究。
【查阅资料】
(1)SO2有毒,常温下是一种无色气体,易溶于水。
(2)酸能使蓝色的石蕊试纸变成红色。
【实验过程】
(1)常温下,实验室用稀硫酸与固体亚硫酸钠反应制取SO2。下列气体的制备装置能用于制备SO2的是(填序号)。
A.加热高锰酸钾制氧气
B.稀盐酸与大理石反应制二氧化碳
C.过氧化氢分解(二氧化锰作催化剂)制氧气
(2)右图A中,实验时,A中蓝色石蕊试纸的颜色始终没有变化,由此得出的结论是。
(3)右图B中,在通入SO2之前,将滴管内的水滴到试纸上,试纸颜色没有发生变化,
由此得出的结论是,当有SO2通过时,湿润的蓝色石蕊试纸变红,由此得出的结论是。
(4)该实验中尾气处理的方法是:将其通入溶液中。
根据下列三组实验回答问题。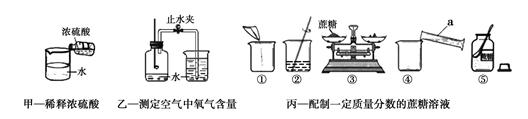
(1)图中仪器a的名称是;三组实验都用到的玻璃仪器是。
(2)指出甲实验中不正确的操作。
(3)乙实验中,燃烧匙中装入的药品应为,其反应的实验现象是。
(4)丙实验中,正确的操作顺序为(填序号):⑤→→→→ ②。