依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量_____________________。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________
(4) 已知下列反应的反应热为:
①CH3COOH(l)+2O2(g)=== 2CO2(g)+2H2O(l) △H=" -" 870.3 kJ• mol-1
②C(s)+O2(g) === CO2(g) △H=" -393.5" kJ• mol-1
③H2(g)+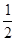 O2(g) === H2O(l) △H=" -" 285.8 kJ• mol-1
O2(g) === H2O(l) △H=" -" 285.8 kJ• mol-1
试写出由C和H2和O2生成CH3COOH的热化学方程式________________________________
(1)下图为实验室制备、收集少量HCl的装置。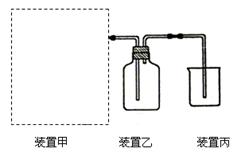
①制备HCl所用药品为浓硫酸和浓盐酸,则甲的最佳装置应选用下图中的。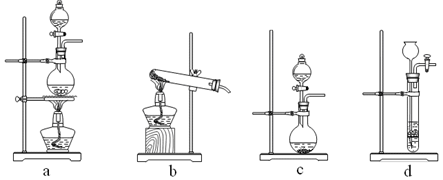
② 请解释能用浓硫酸和浓盐酸制备HCl气体的原因。
③ 装置丙用来吸收过量的HCl气体,为防止倒吸,则烧杯中应该装入水和。
(2)以下为苯的取代反应的探究实验。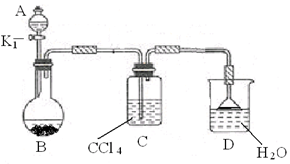
① 按上图所示的装置图连接好各仪器。
② 检验装置的气密性。
③ 在A中加入适量的苯和液溴的混合液体,在B中加入少量铁粉,塞上橡皮塞,打开K1,开始进行反应,放入适量混合液后,关闭K1。
写出B中发生反应的化学方程式。
装置C的作用是。
④ 反应结束后,用试管取少量D中的溶液,加入
(描述试剂和现象),则证明B中的取代反应已经发生。
⑤ 把B中的固液混合物体过滤,分离出液体混合物,按下图方案精制含有苯和溴的溴苯。
其中试剂为 ,操作名称为。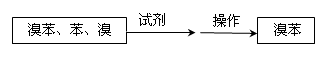
硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:
已知:(ⅰ)PbCl2(s)+2Cl-(aq) PbCl4-(aq)△H>0
PbCl4-(aq)△H>0
(ⅱ)Ksp(PbSO4)=1.08×10-8, Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的PH值分别为3.2、7.04
(1)步骤Ⅰ中生成PbCl2和S的离子方程式,加入盐酸的另一个目的是为了控制PH值在0.5~1.0,原因是。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因。
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式。
(4)请用离子方程式解释滤液2加入H2O2可循环利用的原因,滤液3是。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的 PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为。
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g)
2SO3(g)
(1)此反应是工业上生产的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是(填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
①根据有关数据,请分析在工业生产中选择常压反应器的原因:
。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g)△H=。
2SO3(g)△H=。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下: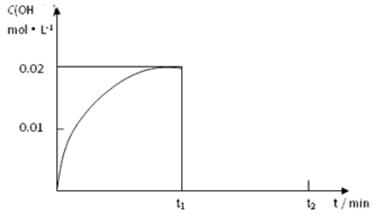
①求该温度时,氨水的电离平衡常数K=。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
① a b(填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3·H2O)=。
(用含有a、b的式子表示)
Heck反应是偶联反应的一种,例如:
反应①: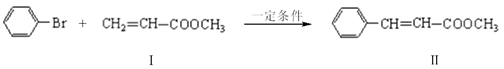
化合物Ⅰ可以由以下途径合成: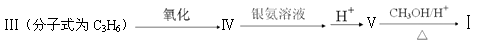
(1)化合物Ⅱ的分子式为,1mol该物质最多可与molH2发生加成反应。
(2)卤代烃CH3CHBrCH3发生消去反应可以生成化合物Ⅲ,相应的化学方程
为(注明条件)。
(3)化合物Ⅳ含有甲基且无支链的同系物Ⅵ的分子式为C4H6O,则化合物Ⅵ的结构简式为。
(4)化合物Ⅴ可与CH3CH2OH发生酯化反应生成化合物Ⅶ,化合物Ⅶ在一定条件下可以发生加聚,则其加聚产物的结构简式为。
(5)化合物Ⅱ的一种同分异构体Ⅷ能发生银镜反应,且核磁共振氢谱只有三组峰,峰面积之比为1:2:2,Ⅷ的结构简式为。
(6)一定条件下,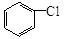 与
与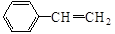 也可以发生类似反应①的反应,其有机产物的结构简式为。
也可以发生类似反应①的反应,其有机产物的结构简式为。
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应
后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色。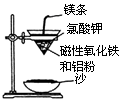
①出现这种现象的原因,除了因“铁块”中可能混有没反应完的
磁性氧化铁外,还有一种可能原因是 。
② 若要证明反应所得“铁块”中含有金属铝,可用(填化学式)溶液,所发生反应的离子方程式为 。
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H+ + 4I-+ O2 = 2I2 + 2H2O。该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率。已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深。
实验小组拟用0.8 mol·L-1 KI溶液、0.1 mol·L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A—C三组实验,部分实验数据如下表:
| 编号 |
温度/℃ |
H2SO4体积/mL |
KI溶液体积/mL |
H2O体积/mL |
淀粉溶液 / mL |
出现蓝色时间 /s |
| A |
39 |
10 |
5 |
5 |
1 |
5 |
| B |
TB |
10 |
5 |
5 |
1 |
没出现蓝色 |
| C |
5 |
10 |
5 |
5 |
1 |
39 |
| D |
t |
①为确保A组实验在39℃下进行,应采用的控温操作方法是。
②A—C三组实验时,都加入了5mL水,其目的是。
③B组实验中“没出现蓝色”,原因是。
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标。
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结
论。