NH3在生活生产中用途广泛。
(1)下列关于NH3或氨水的实验能达到目的的是 (填编号)
| 编号 |
A |
B |
C |
D |
| 实验 装置 |
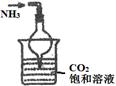 |
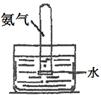 |
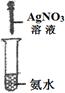 |
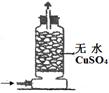 |
| 实验 目的 |
实验室模拟侯氏制碱法制备NH4HCO3 |
验证NH3易溶于水 |
制备银氨溶液 |
干燥NH3 |
(2)利用下图装置(气密性良好)在实验室模拟工业合成氨。
①N2和H2通过A装置,A装置的作用除了将气体混合外,还有 、 作用。
②实验结束,C中溶液有刺激性气味,C溶液中存在的含氮元素的微粒有 。
③某小组消耗大量的N2和H2,但得到的氨水浓度远低于其他组,可能的原因有 。(至少写出一项。注:实验试剂均未变质。)
(3)为验证氨水具有弱碱性,设计了下列实验,其中能达到实验目的是 。(填编号)
A.在氨水中滴入酚酞,溶液变红色
B.测定相同浓度的NaOH和氨水溶液的pH
C.将氨水和过量AlCl3溶液混合,产生白色沉淀
D.用pH试纸测定1mol/L NH4Cl溶液的酸碱性
(4)在实验室初步测定NH3•H2O的电离平衡常数。
①NH3•H2O电离平衡常数的表达式为:K= 。
②限选试剂和仪器:浓度为0.1mol/L 的氨水、0.1000mol/L 盐酸、1.000mol/L 盐酸、酚酞试剂、甲基橙试剂、蒸馏水、酸式滴定管、碱式滴定管、锥形瓶、胶头滴管、pH计、烧杯等(省略夹持仪器)
| 实验步骤 |
实验目的 |
| 步骤1: ①用碱式滴定管取20.00ml 0.1mol/L 的氨水于锥形瓶中,加入几滴 。 ② 。 ③ ,停止滴定,记录数据。重复测定2-3次。 |
测定氨水的准确浓度。 |
| 步骤2: ; |
; |
| 步骤3:通过计算得出氨水的电离常数。 |
X、Y和W为原子序数依次递增的短周期主族元素,X和Y同主族,且能形成气态化合物YX2。试回答下列问题:
(1)W的原子序数为。
(2)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成、再向该试管中加入(填字母),可以看到白色沉淀生成。
A.氨水 B.稀盐酸 C.硝酸钠 D.氯化钙溶液
(3)某小组设计如图所示的装置图(图中夹持和加热装置略去),研究W2的性质。
①装置A、D中观察到的现象分别为、。
②若装置B中装有5.0 mL l.0×10-3 mol·L-1碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为。
(4)若由元素Y和X组成-2价酸根离子M,M中Y和X的质量比为4:3,已知1mol W2与含1mol M的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生。取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。则W2与含M的溶液反应的离子方程式为。
新型陶瓷氮化铝可用Al2O3高温还原法制备: ,用该法制得的产品中常含有少量杂质。某同学拟通过下列实验装置测定产品中AIN的纯度。
,用该法制得的产品中常含有少量杂质。某同学拟通过下列实验装置测定产品中AIN的纯度。
已知:AIN溶于强碱时会生成NH3。
(1)从原料角度分析,AIN中的杂质可能是,装置A中产生气体的化学方程式为。
(2)装置B中的试剂是____;装置C中长颈漏斗的作用是。
在上图右边的方框中,画出所缺装置图,并注明装置中的试剂。
(3)充分反应后,需打开K1,通入一段时间N2,其目的是。
(4)若样品的质量为mg,实验前后装置C增重ng,则样品中AIN昀纯度为。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000 mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入指示剂,进行滴定。滴定至终点,记录数据。
④重复以上过程2次。
试回答下列问题:
(1)应将NaOH溶液注入右图中的(选填“甲”或“乙”)中。
(2)该小组在步骤①中的错误是 ,
由此造成的测定结果  (偏高、偏低或无影响)。
(偏高、偏低或无影响)。
(3)右图是某次滴定时的滴定 管中的液面,右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为mL。
管中的液面,右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为mL。
(4)该滴定操作中③应选用的指示剂是,滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视?,如何确定终点?。
(5)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.52 |
25.42 |
| 第二次 |
20.00 |
4.07 |
29.17 |
请计算待测烧碱溶液的浓度为。
(6)如有1mol/L和0.1mol/L的HCl溶液,应用_ _的HCl溶液,原因是_________。
(共8分)抗击“非典”期间,过氧乙酸(CH3COOOH)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
①□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
②H2O2+2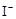 +2H+ =I2+2H2O
+2H+ =I2+2H2O
③CH3COOOH+2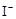 +2H+= CH3COOH+I2+H2O
+2H+= CH3COOH+I2+H2O
④I2+ 2S2O32- =2I-+ S4O62-
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填入以下方框内):
□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
(2)用双线桥法在下面已配平的化学方程式上标出电子转移的方向和数目:
□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
(3)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是____________________。
(4)取b0 L待测液,用硫酸使溶液酸化,再用浓度为a1 mol· 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol·
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol· 的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 L。请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。c0= _______________ mol·
的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 L。请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。c0= _______________ mol· 。
。
(5)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 ________(填是或否)
(14分)某同学设计如图装置,研究非金属元素性质变化规律。
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,一般地,强酸能制弱酸,现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2Si O3。
O3。
A中装试剂________,B中装试剂________,C中装试剂________。C中实验现象为__________;写出C中发生反应的离子方程式______________________________________。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用如图装置证明氯气氧化性强于碘单质的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末,C中装试剂________,C中现象______________________。写出离子方程式________________________________。该实验该装置有明显不足,请指出改进方法:_____________________________________________。
(3)如果C中装饱和的氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,写出化学方程式________________________________;
证明氯的非金属性比硫的非金属性________(填“强”“弱”或“无法判断”)。