在室温下,化学反应I–(aq) + OCl–(aq)=OI–(aq) + Cl–(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
| 实验编号 |
I–的初始浓度 (mol·L-1) |
OCl–的初始浓度 (mol·L-1) |
OH–的初始浓度 (mol·L-1) |
初始速率v (mol·L-1· s-1) |
| 1 |
2 × 10–3 |
1.5 × 10–3 |
1.00 |
1.8 × 10–4 |
| 2 |
a |
1.5 × 10–3 |
1.00 |
3.6 × 10–4 |
| 3 |
2 × 10–3 |
3 × 10–3 |
2.00 |
1.8 × 10–4 |
| 4 |
4 × 10–3 |
3 × 10–3 |
1.00 |
7.2 × 10–4 |
已知表中初始反应速率与有关离子浓度关系可以表示为v=" k" [I–]1 [OCl–]b [OH–]c(温 度一定时,k为常数)
①为了实施实验1,某同学取5mL0.02mol·L-1碘化钾溶液、5mL0.015 mol·L-1次氯酸钠溶液、40mL某浓度氢氧化钠溶液混合反应。则该氢氧化钠溶液物质的量浓度为 _________ mol·L-1;
②实验2中,a= ;
③设计实验2和实验4的目的是 ;
④计算b、c值:b= ;c=
⑤若实验编号4的其它浓度不变,仅将溶液的OH–的初始浓度变为0.1mol·L-1,反应的初始速率v=
(mol·L-1· s-1)。
(14分)今有aX、bY、cZ三种元素。
已知:
①各原子序数a、b、c均小于20,且a+b+c=25;
②元素Y的原子外围电子构型为ns2npn+2;
③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物;
④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38:77。
据上可推知,
(1)X、Y、Z三种元素形成的常见化合物的化学式是_________________。
(2)X2Y2是________晶体(填晶体类型),构成晶体的微粒是________(填微粒符号) ,该晶体中微粒间的作用有__________________________________。
(3)Z的硫化物和氯化物的分子空间构型分别是____________、__________,其中Z原子分别以______杂化轨道成键,根据成键方式分类,Z的硫化物分子中含有的键的种类及其数目是______________。
(4)Z的氢化物种类很多,写出Z的氢化物分子中所有原子都在同一平面上的任意两种简单的化合物的名称_________、__________。
(11分)下图是元素周期表的一部分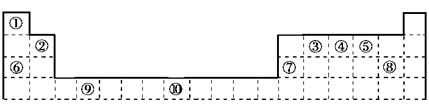
(1)写出元素⑩的基态原子的电子排布简化式________,外围电子排布图________________。指出它在周期表中的位置________。焊接钢轨时,常利用⑩的某些氧化物与⑦的单质在高温下发生反应,试写出其中一条反应的化学方程式_____________________________。
(2)①③⑤三种元素可以形成多种有机化合物分子,其中最简单原子数最少的一种是室内装潢时形成的主要气体污染物。试写出它的电子式________,推测该分子的空间构型为________。
(3)③④⑤⑥⑧五种元素都可以与元素①形成化合物,其中熔点最高的是________(写化合物的化学式)。如果在温度接近373 K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果总是比理论值高,其原因是___________________________________________。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式___________________________。
(14分,每空2分)有A、B、C、D 4种烃,各取0.01 mol充分燃烧后,B、C、D所产生的二氧化碳均为448 mL(标准状况);A燃烧所得的二氧化碳是其他三者的3倍。在镍催化剂的作用下,A、B、C都能和氢气发生加成反应,B可以转变为C或D,C可以转变为D;B或C都能使酸性高锰酸钾溶液褪色,而A、D无此性质;在FeBr3存在时,A与溴发生取代反应。
试推断出4种烃的结构简式:
(1)A是_______________,B是______________,C是______________,D是________________。
(2)B→D的反应方程式:_____________________________________________。
(3)除去D中C的反应方程式:______________________________________。
(4)C发生加聚反应的方程式:________________________________________。
(12分,每空2分)某研究性学习小组的课题为“Mg—Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如下图所示(C1、C2均为碳棒),按要求填写下列空格。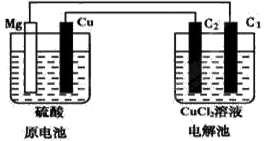
(1)铜片上的现象是,该极的电极反应式为。
(2)C1极的名称为,C2极的电极反应式为。
(3)下列关于该装置中电子流向的叙述中正确的是。
| A.从镁电极经导线流向C1极 |
| B.从C1极经导线流向镁电极 |
| C.从铜电极经导线流向C2极 |
| D.从C2极经导线流向铜电极 |
(4)原电池中稀硫酸的体积为200 mL ,物质的量浓度为1.5 mol·L-1,当电解池中某碳棒上产生3.36 L(标准状况)气体时,求:
①有个电子通过了电线(NA=6.02×1023) 。
②此时原电池溶液中H+的物质的量浓度为mol/L(不考虑溶液体积变化)。
(14分,每空2分)向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应
SO2(g)+NO2(g) SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
(1)点a-c段,速率变化的主要原因是,点c后速率变化的主要原因是。
(2)c点是否已经达到平衡状态(填“是”、 “否”或“不一定”)
(3)反应物浓度:a点b点(填“<”、“=”或“>”)
(4)反应物的总能量生成物的总能量(填“<”、“=”或“>”)
(5)△t1=△t2时,SO2物质的量的变化量:a~b段b~c段(填“<”、“=”或“>”)