硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。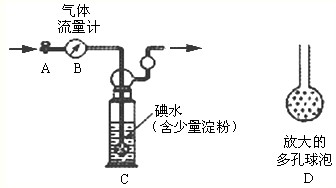
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是 。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种: 。
(3)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”、“偏低” 或“无影响”)。
乙方案:实验步骤如下面流程图所示:
(4)写出步骤②中反应的化学方程式 。
(5)步骤③中洗涤沉淀的方法是 。
(6)通过的尾气体积为VL已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为
(用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液中,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由: 。
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”。某学校化学科研小组现对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:资料表明:谷氨酸钠的存在不影响NaCl含量进行测定。
Ⅱ.设计实验方案:
(1)实验原理:。
(2)实验试剂:水、试剂X的溶液等
(3)实验过程: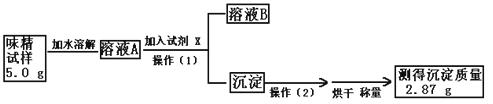
根据上述实验步骤回答下列有关问题:
①.操作(1)所需要的玻璃仪器有。
②.操作(2)的名称为:。
③.通过计算判断该味精中NaCl的质量分数,是否符合其包装上标注的标准。
_______ (填“符合”或“不符合”)
④.计算实验操作(1)所得溶液为50 mL,则溶液A中NaCl的物质的量浓度是
(第③④问写出必要的计算过程)
某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质。请回答下列问题: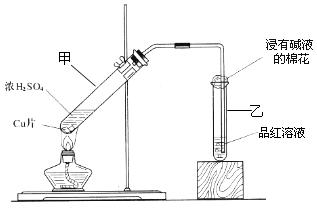
(1)通过试管乙中发生的 现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有 性。
(2)写出试管甲中所发生反应的化学方程式,并标明电子转移方向和数目。
。
(3)试管乙口部浸有碱液的棉花的作用是 ,此防范措施也说明产生的气体是 (填“酸性”、“中性”或“碱性”)气体, (填“有”或“无”)毒性。
(4)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水V L,加入0.5 mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算:
①该雨水中共溶解SO2的体积是 mL(标准状况)。
②若生成沉淀物的质量为4.50 g,则沉淀物的组成为 (填写化学式)。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下: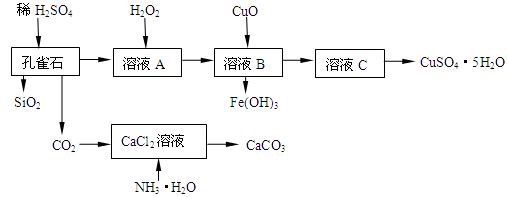
试回答下列问题:
(1)在未加入H2O2的溶液A中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是 (填代号)。
| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
向溶液A中加入H2O2,H2O2在该反应中作氧化剂。实验室选用H2O2而不用Cl2作氧化剂。除考虑环保因素外,另一原因是不引入杂质 离子。
(2)由溶液C获得CuSO4·5H2O,需要经过加热浓缩, ,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(3)制备CaCO3时,发生反应的化学方程式是 ;若实验过程中有氨气逸出,可选用下列装置中的 (填代号)装置吸收氨气。
(烧杯中的液体都为水)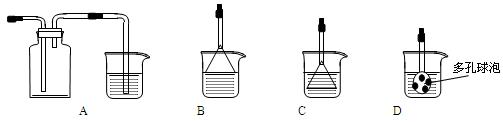
(4)欲测定溶液A中Fe2+的浓度,需配制100 mL 0.1 mol∕LKMnO4标准溶液。配制该溶液时:除烧杯、玻璃棒、胶头滴管外,还需的一种玻璃仪器是 ;当往该玻璃仪器中加蒸馏水至接近刻度线1-2cm时,应改用 滴加蒸馏水至溶液的凹液面正好与刻度线相平。
纯铁在冷的浓硫酸中能发生钝化。某兴趣小组同学发现将一定量的纯铁与浓硫酸加热时,铁完全溶解,得到溶液A,并产生大量气体B。实验室现有下列试剂:0 .01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分,并将有关实验操作、预期现象和结论填入下列表格中。
.01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分,并将有关实验操作、预期现象和结论填入下列表格中。
[提出猜想]
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有中的一种或两种。
Ⅲ.任意写出一个铁与浓硫酸加热时,可能发生的有关反应方程式
[实验探究]
实验操作 |
预期现象 |
结论 |
|
| 验证猜想Ⅰ |
步骤①:取少量溶液A,滴入0.01 mol/L 酸性KMnO4溶液 |
||
| 步骤②: |
含有Fe3+ |
||
| 验证猜想Ⅱ |
将所得气体B通入如下图装置 |
含有两种气体 |
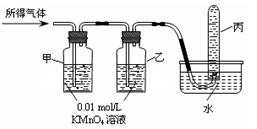
[问题讨论]
有同学提出,若另外选用KSCN溶液,则
仅利用KSCN和H2O2两种溶液即可完成
猜想Ⅰ的所有探究,请对该观点进行评价:
。
某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙两套装置(图中的夹持仪器均未画出,"△"表示酒精灯热源),每套装置又可划分为①、②  、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b
、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b  -铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。
-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。 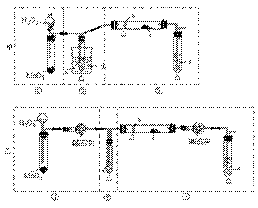
(1)对比两套方案,简述各自的优点:
甲_______________________________
________________________________。
乙_______________________________
________________________________。
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为1.甲①(接干燥管) 2. _______ 3. _______(例如甲①,乙②)
(3)实验中钢丝的作用是_________________。
(4)实验中能验证乙醇氧化产物的实验现象是______________________________________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式_________________________。