常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
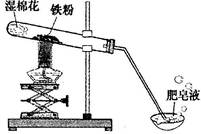
(1)试管尾部放一团湿棉花的目的是
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。 说明生成的气体是
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 |
|
|
|
| 颜色、状态 |
黑色粉末 |
红棕色粉末 |
黑色晶体 |
| 能否被磁铁吸引 |
否 |
否 |
能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是
与
;猜想二:剩余固体是
【实验探究】
| 实验操作 |
实验现象及结论 |
|
|
|
【实验结论】铁和水蒸气反应的化学方程式为
【反思与交流】该黑色固体不可能是
,理由是
【2015年上海市】实验室常用的制取气体的发生装置如下: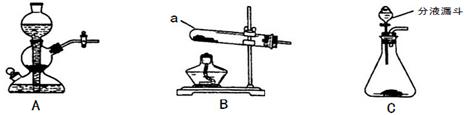
①仪器a的名称是 ;搭建B装置时,酒精灯应在固定仪器a之 (选填“前”或“后”)放置。
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是 。
③在实验室制取二氧化碳的研究中,进行了如下实验:
| 药品 实验编号 |
甲 |
乙 |
丙 |
丁 |
| 大理石 |
m g,块状 |
m g,块状 |
m g,粉末状 |
m g,粉末状 |
| 盐酸(过量) |
w g,稀盐酸 |
w g,浓盐酸 |
w g,稀盐酸 |
w g,浓盐酸 |
I.上述实验中反应的化学方程式是
II.若要研究盐酸浓度大小对反应的影响,可选择实验甲与 对照(选填实验编号)。
III.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是 。
IV.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是 (选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳地产生。请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因。网
| 目的 |
原料 |
发生装置 |
气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 |
块状大理石 稀盐酸 |
A |
|
| 制取氧气 |
粉末状二氧化碳 3%的过氧化氢溶液 |
B |
|
【2015贵州省安顺市】竹炭包是一种集观赏与空气净化为一体的产品。这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行吸附。某课外活动小组对竹炭进行初步探究。
【提 出 问题】竹炭中是否含有碳元素
【猜想与假设】竹炭中含有碳元素
【查 阅 资料】新鲜的血液,遇一氧化碳由鲜红变为暗红。
【设 计 实验】所用装置如下图所示。(A装置的作用为吸收空气中的水和二氧化碳)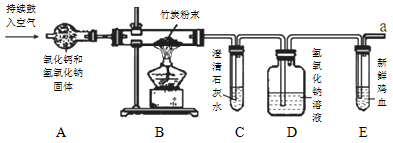
(1)实验开始后,C装置中产生白色沉淀,发生反应的化学方程式为 ,E装置中新鲜的鸡血变为暗红色。
(2)小玥认为应在A、B装置间,再增加一个C装置,目的是 。
(3)课外活动小组的同学设计的这套装置的不足之处是 ,请你设计解决的方法 。
(4)小亮认为可以用右图所示的装置,替换原装置中的E装置,
你认为 (填“可以”或“不可以”),原因是 。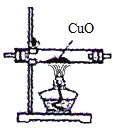
【结论】竹炭中含有碳元素。
【拓展应用】竹炭细密多孔,竹炭牙膏中含有竹炭等成分具有消炎、止痛、化淤、去污等功效,下列有关竹炭牙膏的用途描述不正确的是 。
A、可除衣领袖口等处的汗渍B、不能除去口中异味C、虫咬、灼伤可消炎止痛
【2015年广东省】“题23图”为某家长带小孩在下水道井盖小孔上点燃鞭炮发生爆炸的画面。现要探究某下水道的可燃性气体成分:
【猜想】(I)含可燃性气体CO;(II)含可燃性气体CH4;
(III)含可燃性气体CO和CH4 。
【收集气体】用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,使 ,将瓶提到井口迅速盖好瓶备用。
【进行实验】
| 步骤 |
实验搡作 |
实验现象 |
结论 |
| ⑴ |
导出瓶中气体,,通过装有 的洗气瓶。 |
 |
目的是除CO2等 酸性气体。 |
| ⑵ |
再通过装有浓硫酸的洗气瓶。 |
 |
目的是除去 。 |
| 将步骤(2)的气体导出点燃; ①用吸附少量无水硫酸铜粉末的石棉贴在小烧杯内壁,再把小烧杯斜罩于火焰上方; ②用内壁粘有澄清石灰水的小烧杯罩于火焰上方。 |
无水硫酸铜 ; ‚烧杯内壁变浑浊。 |
证明有H2O生成; ‚证明有 生成。 |
【作出判断】根据上述实验现象,甲同学认为猜想III正确;而乙同学认为甲的判断不严谨。
因为猜想 也有相同的现象。如需进一步确认还应检验 的存在,
其方法是 。
【拓展】若需要工人进入下水道清理淤泥,打开下水道井盖后应首先进行的操作是 。
【2015年上海市】甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。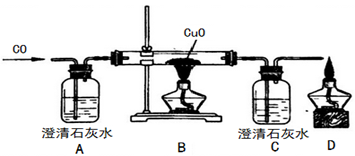
①B中反应的化学方程式是 ,该反应的还原剂是 。
②实验过程中,C中的现象是 ,D处点燃的目的是 。
③对该实验的分析正确的是 (选填编号)
a、实验结束时应先熄灭B处酒精灯
b、C中增加的质量与B中固体减少的质量相等
c、反应开始后通入0.1mol一氧化碳可生成0.1mol铜
d、反应结束后继续通入一氧化碳的目的是防止铜被氧化
④甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,理由是 。
【2015年福建省厦门市】“史上最贵”的实验:
步骤Ⅰ.让金刚石在充足的氧气中燃烧,收集生成的气体;
步骤Ⅱ.让足量镁条在步骤Ⅰ生成的气体中燃烧,生成黑色的炭粉和白色的固体氧化物。
(1)步骤Ⅱ中发生反应的化学方程式:___________________,基本反应类型是_________。
(2)若金刚石质量为m1,按上述步骤反应且转化完全,生成的炭粉质量为m2,则m1____m2(填“<”、“=”、“>”=,理由为___________________________________________。