(9分)如下图装置实验,A、B两烧杯分别盛放200 g10%NaOH和足量CuSO4溶液。通电一段时间后,c极上有Cu析出,又测得A杯中溶液的质量减少4.5 g(不考虑水的蒸发)。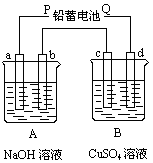
请回答下列问题:
(1)电源P极为 极;请分别写出b极和c极上发生的电极反应 式: ;
(2)c极上析出固体铜的质量为 g
(3)若装置中用铅蓄电池作电源,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
假设在a极制得气体0.050 mol,这时电池内消耗的H2SO4的物质的量至少是 mol
(1)某温度(t℃)时,水的Kw=10-13mol2·L-2,则该温度(填大于、小于或等于) 25℃,其理由是 。
(2)将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,则:
①若所得混合液为中性,则a∶b=;
②若所得混合液的pH=2,则a∶b=;
1)相同物质的量浓度下的各溶液:NaX、NaY、NaZ,其PH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序为:
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是
(3)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a b相连,a为负极;c d相连,c为负极;a c相连,c为正极;b d相连,b为正极,则四种金属的活动性由强到弱顺序为:
(4)写出Na2CO3溶于水后的电离方程式: ________________________________________________________
(5)写出氯化铁溶液水解反应的离子方程式: ______________________________________________
A、B、C、D四种短周期元素,原子序数依次增大,A元素原子最外层电子数是次外层的2倍,0.05 mol B元素的离子得到的6.02×1022个电子后被还原为中性原子;0.4g B的氧化物恰好与100mL 0 .2mol/L的盐酸完全反应;B元素原子核内质子数与中子数相等。C离子核外电子层数比A元素的离子核外电子层数多1,且形成离子化合物BC,D与A可形成化合物。请填空:
.2mol/L的盐酸完全反应;B元素原子核内质子数与中子数相等。C离子核外电子层数比A元素的离子核外电子层数多1,且形成离子化合物BC,D与A可形成化合物。请填空:
(1)A、B 两种元素的元素符号:B___________ 、C__________。
(2)D与A形成化合物分子式是________,分子空间构型是________。
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)写出元素符号:X、Y、Z、W
(2)ZW2的电子式是,它在常温下呈液态,形成晶体时,属于晶体。
(3)工业生产单质Y的原理是(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是。
(5)0.1mol的单质W与50mL1.5mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是。
根据已有内容的规律进行增补
(1)填化学方程式:
①2Na+2H2O=2NaOH+H2↑
②2HBr+Cl2=2HCl+Br2[
③2H2S+O2=2S+2H2O
④____________________________。
(2)已知
| 化学键 |
Si-O |
Si-Cl |
H-Cl |
Si-Si |
| 键能/KJ·mol-1 |
460 |
360 |
431 |
176 |
回答下列问题:
①比较熔点SiCl4SiO2(填“>”或“<” ),理由
②工业制纯硅反应如下:
1/2 SiCl4(g)+H2(g)="=" 1/2Si(s)+2HCl(g)△H= +118KJ·mol-1
则H-H键能为KJ·mol-1