A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E 、G ;F在元素周期表中的位置是 .
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是 。
(3) E在D2中燃烧生成化合物X中阴阳离子个数比为 ;X中的阴离子电子式为 .
(4)能够说明可逆反应2CD2(g)  C2D4(g)达到平衡状态的标志是 ;
C2D4(g)达到平衡状态的标志是 ;
①单位时间消耗2mol CD2的同时,生成1 mol C2D4②恒温恒压下,混合气体的密度不变③CD2和C2D4的浓度之比为2∶1 ④混合气体的颜色不变⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5 mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为 。
活性氧化锌在橡胶、化工、涂料、陶瓷、医药、电子等行业有着广泛的应用。但随着锌资源的不断开发和利用,锌矿资源越来越少,因此研究利用锌二次资源对缓解锌资源枯竭进程具有重要意义。下图是以含锌铜烟尘(火法炼铜的副产品,主要成分是ZnO、CuO和FeO)制备活性氧化锌的工艺流程: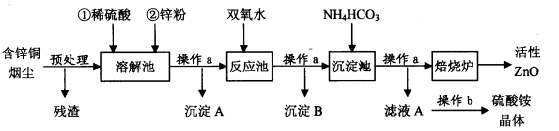
含锌铜烟尘经过预处理后的主要成分为ZnO,还含有少量的CuO和Fe2O3。
(1)操作a名称是____,在实验室中,该过程用到的主要玻璃仪器有。
(2)溶解池中待固体全部溶解后,加入锌粉的作用有:
①将Fe3+还原为Fe2+;②:③调节溶液的pH(控制其在5,0-5.4之间)。
(3)检验溶解池中Fe3+已全部被还原为Fe2+的最佳试剂是;
(4)右表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为
1.0 mol-l计算)。反应池中的温度控制在90-95℃,请写出反应池中所发生反应的离子方
程式:。
| 开始沉淀的pH |
沉淀完全的pH |
|
| Fe3+ |
1.1 |
3.2 |
| Fe2+ |
5.8 |
8.8 |
| 2n2+ |
5.9 |
8.9 |
(5)操作b的名称是________;
(6)沉淀池中得到的沉淀化学式可以表示为:aZnCO3·bZn(OH)2·cH2O(a、b、c均为整数)。某校化学兴趣小组的同学为了确定其组成,进行如下实验:称取3.59g沉淀进行焙烧,将焙烧过程中产生的气体依次通过足量的浓硫酸和碱石灰,它们分别增重0.72g和0.44g,则该沉淀的组成为。
水泥是一种重要的建筑材料,水泥的强度是评价水泥质量的重要指标,它与水泥中CaO的含量有着良好的相关性,因此在特殊情况下可以通过测定其中Ca0的含量预测水泥的强度。为测量某品牌水泥中氧化钙的含量,进行如下实验:
步骤1:熔样:准确称取0.3000g试样置于坩埚中,高温灼烧5分钟后,冷却并研碎,加入2.000g无水碳酸钠混匀后,再高温灼烧10分钟。
步骤2:酸溶:取冷却后的烧结块,加入40mL水后,再加入l0mL稀盐酸和3滴稀硝酸。
步骤3:除杂:在酸溶后所得溶液中慢慢滴加稀氨水使其中的Fe3+、Al3+转化为沉淀,过滤。
步骤4:沉淀:在滤液中加入草酸铵溶液,加热煮沸后,边搅拌边滴加氨水至弱碱性,静置。
步骤5:溶解:将生成的草酸钙( CaC2O4)沉淀加入到稀硫酸中,加热并搅拌使其完全溶解。
步骤6:滴定:用0.1000 mol·L-1的KMnO4溶液进行滴定至微红色出现并保持30s不消失,共用去KMnO4溶液13.000mL。反应的化学方程式为:2 KMnO4+5 H2C2O4+3H2SO4= K2SO4+2MnSO4+5CO2↑+8H2O
(1)写出步骤3中Al3+转化为沉淀的离子方程式:;
(2)已知室温下Al(OH)3的Ksp=1.0×10-33,欲使溶液中c(Al3+)≤l.0xl0-6mol·L-1,pH≥;
(3)通过计算确定该试样中氧化钙的质量分数(写出计算过程)。
以化合物A为原料合成化合物M的线路如下图所示:
已知: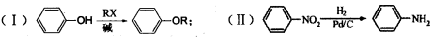
(1)写出下列反应的反应类型:反应①:;反应④:。
(2)写出化合物B中含氧官能团的名称:和。
(3)反应⑤中除生成M外,还有CH3OH生成。请写出物质A和Y的结构简式:
AY。
(4)写出同时满足下列条件的B的两种同分异构体的结构简式:和。
I.分子中含有苯环结构:
II.分子中有4种不同化学环境的氢:
Ⅲ.既能与FeCI3溶液发生显色反应,也能发生银镜反应
(5)反应②和反应③的次序不能颠倒,其原因是。
氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体。
(1)液氨和水类似,也能发生电离:NH3+NH3 NH4++NH2-,其离子积常数为l.0xl0-30。现将2.3g金属钠投入1.0 L液氨中,则液氨电离平衡____移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为____。
NH4++NH2-,其离子积常数为l.0xl0-30。现将2.3g金属钠投入1.0 L液氨中,则液氨电离平衡____移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为____。
(2)实验室模拟工业上用氮气和氢气合成氨气时,在反应前将两种气体通过图装置,该装置的作用有三个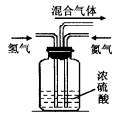
①将氮气和氢气干燥:
②使氮气和氢气充分混合;
③____,从而提高氮气和氢气的利用率。
(3)实验室可用氨气通过红热的氧化铜制取氮气,写出该反应的化学方程式:____。
(4)家庭空气中的氨主要来自建筑施工中使用的混凝土外加剂,如混凝土防冻剂尿素会和水缓慢发生反应:CO(NH2)2(s)+H2O(g) 2NH3(g) +CO2(g),该反应的平衡常数表达式为K=。
2NH3(g) +CO2(g),该反应的平衡常数表达式为K=。
(5)已知:N2(g)+O2(g)=2NO(g); △H=180Kj·mol-l
4NH3(g)+5O2(g) =4NO(g)+6H2O(g); △H= -908Kj·mol-l
请写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式:。
(10分)偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l) 2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g) 2NO2(g) (Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为(填“吸热”或“放热”)反应。
2NO2(g) (Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是。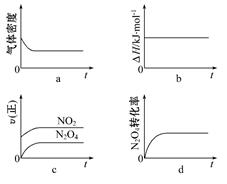
若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数(填“增大”、“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0 s~3 s内的平均反应速率v(N2O4)=mol·L-1·s-1。