下列各个曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中: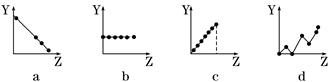
(1)ⅡA族元素的最外层电子数________;
(2)第3周期元素的最高化合价________;
(3)F-、Na+、Mg2+、Al3+的离子半径________。
糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_____________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和____________(写结构简式或名称)。人体中共有二十多种氨基酸,其中人体自身_______________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:_______________。
(4)蛋白质在一定条件下能发生变性,从而失去生理活性。万一误服硫酸铜溶液,此时应立即作怎样的处理? 。
2008年9月25日21时10分,我国在酒泉卫星发射基地成功发射神舟七号宇宙飞船,实现了中国航天航空史上的伟大突破。承载神舟七号升空任务的是长征二号F型火箭,其第一节、第二节、第三节均以液态四氧化二氮(N2O4)和联氨(N2H4)为原料,使后者在前者中燃烧,产生巨大的推动力助火箭升空,最终产物是N2和H2O。
(1)请写出该反应的化学方程式_______________________;
(2)反应中氧化剂是____________________;
(3)该反应属于_______________(填“放热反应”或“ 吸热反应”)。
(1)0.1molO2中,含有 mol O;
(2)标准状况下,67.2L Cl2的物质的量为 mol;
(3)4gNaOH固体的物质的量为 mol,将其溶于水配成500mL溶液,此溶液中NaOH的物质的量浓度为
(1)某澄清透明溶液,可能含有下列离子:Fe3+ 、K+、Ba2+、Al3+、NH4+、Cl-、NO3-、SO42-。现做以下实验:
①取少量溶液,加入用稀HNO3酸化的BaCl2溶液,产生白色沉淀。
②另取溶液,逐滴加入NaOH溶液至过量,只看到有红棕色沉淀生成且沉淀质量不减少。
由此可以推断:溶液中肯定存在的离子有 ;溶液中肯定不存在的离子有 ;溶液中不能确定是否存在的离子有 ;
(2)制备Fe(OH)2时,向FeSO4溶液中滴加NaOH溶液时,滴管尖端的位置是 _ ;原因是: 。
已知某些金属氧化物跟熔融烧碱反应可生成盐。根据下列框图填空。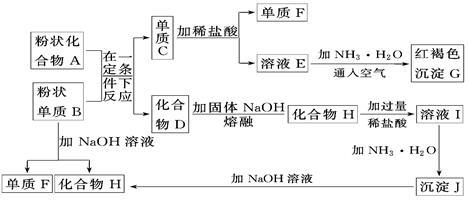
(1)单质C是______________、化合物H是______________
(2)写出由E生成G的离子反应方程式________________________。
(3)溶液I中所含金属离子是________________________________。