长郡中学某化学兴趣小组设计如图所示的实验装置来探究隔绝空气加热后亚硫酸钠分解后的产物(查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解)。
(1)如何检查上述装置的气密性____________________________________________________。
(2)如果加热温度低于600℃,向所得冷却后固体试样中滴加70%硫酸至足量,在装置B中观察到的现象为_______________________________________________________________,此时A中反应的离子方程式为:______________________________________________。
(3)当加热温度为600℃以上一会儿后,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,同时发现在B中无明显现象,C中发现有黑色沉淀产生,则生成淡黄色沉淀的离子方程式为_________________________________________________。
(4)在(3)中滴加足量稀盐酸后,烧瓶内除Cl-外,还存在另一种浓度较大的阴离子。请简述检验该离子的方法:____________________________________________________________。
(5)写出Na2SO3固体加热到600℃以上分解的化学方程式:_________________________。
S2Cl2是一种易挥发的液体(熔点:—76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置 (夹持装置、加热装置均已略去)。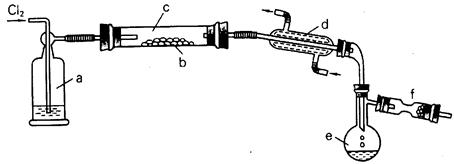
(1)已知S2Cl2分子结构与H2O2相似,则S2Cl2的分子中共含有条共价键。
(2)装置a中应放试剂为 ;装置d的名称是 ,它的作用是。
(3)该实验的操作顺序应为 (用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2⑤停止加热装置c
(4)图中f装置中应放置的试剂为 ,其作用为。
(5)将S2Cl2的水解气体产物通入氯水中,若观察到的现象,则可证明水解产物中有硫化氢生成。
二氧化硫和氮的氧化物是重要的化工原料,同时也是造成大气污染的主要物质。对其性质的研究是化学的重要任务。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)N2O5在四氯化碳溶液中的分解反应为:2N2O5=4NO2+O2。实验测得在67℃时反应体系中N2O5的物质的量浓度随时间的变化如下表所示。
| t/min |
0 |
1 |
2 |
3 |
4 |
5 |
| c(N2O5)/mol·L—1 |
1.00 |
0.71 |
0.50 |
0.35 |
0.25 |
0.17 |
①实验进行的前1分钟和最后1分钟,用N2O5的物质的量浓度变化表示的平均反应速率分别是、。
②实验进行的最后1分钟,用NO2的物质的量浓度变化表示的平均反应速率是;5分钟时NO2的物质的量浓度是。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中放出的热量为____kJ。
I、实验室中常以BaSO4重量法测定BaCl2·nH2O中的Ba的含量主要步骤如下:
①灼烧瓷坩埚至恒重,称得坩埚的质量
② 称取BaCl2·nH2O并在烧杯中溶解,加盐酸处理
③ 将一定浓度的过量硫酸滴入钡盐中得到白色沉淀
④ 静置,
⑤ 将沉淀和滤纸置于瓷坩埚中,经酒精喷灯加热碳化后,继续在800-850℃灼烧至恒重,称重
⑥ 计算
请回答下列问题:
(1)省略第①步中“灼烧瓷坩埚至恒重”可能导致计算结果_ ______(填“偏高”、“不变”或“偏低”)。
______(填“偏高”、“不变”或“偏低”)。
(2)第④步静置后的操作是。
(3)第⑤步灼烧温度不超过900℃,是因为_______________________。
II、某同学用氨水吸收一定量的SO2,吸收后溶液中可能含有OH-、SO32-、SO42-、 HSO3- 等阴离子中的若干种。
(4)写出氨水吸收过量SO2的反应的离子方程式:
(5)已知亚硫酸氢盐一般可溶于水。仅限选择的仪器和试剂:烧杯、试管、玻璃棒、胶头滴管; 2 mol/L盐酸、2 mol/L硝酸、1 mol/L氯化钡溶液、l mol/L氢氧化钡溶液、品红溶液、蒸馏水。请设计实验探究吸收后溶液中是否存在SO32-、HSO3-,将实验操作、预期的实验现象和结论填在下表中。
| 实验操作 |
预期现象与结论 |
| 步骤1:取少量待测液放入试管1中,滴加过量lmol/L氯化钡溶液。 |
若不出现浑浊,则溶液中不存在SO32-, 若出现浑浊,则溶液中可能含有SO32-。 |
| 步骤2:若出现浑浊,静置一段时间后,将上层清液倒入试管2中。往试管1中加入蒸馏水洗涤沉淀,静置后弃去上层清液,再加入。 |
|
| 步骤3: |
(14分)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
[甲方案]:如图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。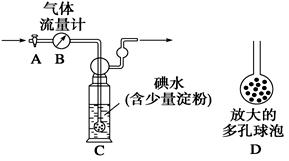
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是_______________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量____________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示:
(3)步骤①中过量H2O2的作用是
(4)写出步骤②中反应的化学方程式_______________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是________________________________
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为__________________________(用含有V、m的代数式表示)。
(12分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。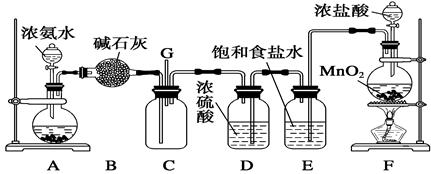
请回答下列问题:
(1)装置F中发生反应的离子方程式为____________________________________________。
(2) B装置的名称是___________________;E装置的作用___________________________。
(3)通入C装置的两根导管左边较长、右边较短,目的是____________________________。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:__________________________________________________。