我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成加合物H2NCONH2·H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体经测定H2O2结构如图所示,结合以上信息,下列说法不正确的是
| A.任何分子式中的“· ”都表示氢键 |
| B.H2O2是极性分子,其结构简式为HO—OH |
| C.H2O2既有氧化性又有还原性 |
| D.H2NCONH2与H2O2是通过氢键结合的 |
关于氨水的叙述中错误的是( )
| A.氨水的主要成分是NH3·H2O |
| B.氨水可使酚酞指示剂变红 |
| C.氨水中含三种分子和两种离子 |
| D.氨水中溶质的质量分数越大,溶液密度越小 |
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32—、SO42—,现取三份各100 mL溶液分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g.根据上述实验,以下推测正确的是( )
| A.K+一定存在 |
| B.100 mL溶液中含0.01 mol CO32— |
| C.Cl-一定存在 |
| D.Ba2+一定不存在,Mg2+可能存在 |
在a L Al2(SO4)3和(NH4)2SO4的混合物溶液中加入b mol BaCl2,恰好使溶液中的SO完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度为( )
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质:
①Cu和HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
由于浓度不同而能发生不同氧化还原反应的是( )
| A.①③ | B.③④ | C.①② | D.①③④ |
制造太阳能电池需要高纯度的硅,工业上制高纯度硅常用以下反应来实现:(1)Si(粗)+3HCl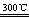 SiHCl3+H2,(2)SiHCl3+H2
SiHCl3+H2,(2)SiHCl3+H2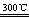 Si+3HCl.对上述两个反应的下列叙述中,错误的是( )
Si+3HCl.对上述两个反应的下列叙述中,错误的是( )
| A.两个反应都是置换反应 |
| B.两个反应中的H2均为还原剂 |
| C.两个反应的条件不同 |
| D.两个反应都是氧化还原反应 |