某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置实验来验证卤族元素性质的递变规律(夹持装置已略去)。A、B、C三个胶头滴管分别是氯酸钾溶液、NaBr溶液、淀粉KI溶液。已知常温下浓盐酸与氯酸钾溶液能反应生成氯气。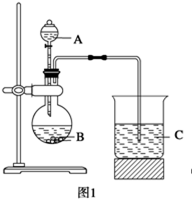
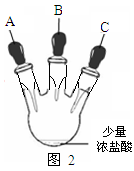
(1)甲同学设计实验所涉及的离子方程式为_________________、_______________;
(2)乙同学具体操作如下:
①先挤压胶体滴管A,使少量溶液滴入烧瓶内,可观察到 ;
②挤压体滴管B,使稍过量溶液滴入烧瓶内,充分反应。写出该操作中主要离子方程式为 。
③再挤压体滴管C,使少量溶液滴入烧瓶内,可观到 ;
(3)根据甲乙同学的实验可得到的结论是: 。
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题: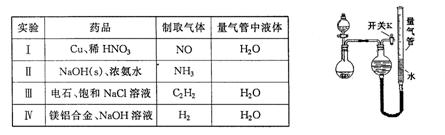
(1)实验过程中,使用分液漏斗滴加液体的操作是。
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”),原因是。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是,打开开关K,产生的气体经验纯后点燃,现象是。
(4)实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有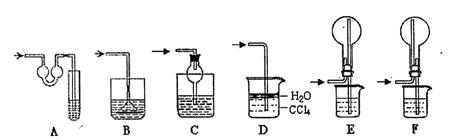
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 |
镁铝合金度量 |
量气管第一次读数 |
量气管第二次读数 |
| ① |
1.0g |
10.0mL |
346.3mL |
| ② |
1.0g |
10 .0mL .0mL |
335.0mL |
| ③ |
1.0g |
10.0mL |
345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为____。
某研究性学习小组利用下图所示装置研究乙醇与氧化铁的反应,请回答下列问题:
(1)装置中试管B的作用是。
(2)实验中可观察到石英管A中的现象为。
(3)反应停止后,取出试管C在酒精灯上加热至沸腾,可观察到有红色沉淀产生。写出该反应的化学方程式。
(4)为了测定反应后石英管A左侧固体中铁元素的含量,进行如下实验: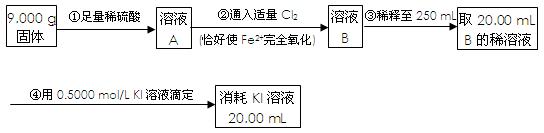
(i)步骤③中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、。
(ii)下列有关步骤④的操作中说法正确的是。
a.滴定过程中可利用淀粉溶液作为指示剂
b.滴定管用蒸馏水洗涤后可以直接装液
c.锥形瓶不需要用待测夜润洗
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
(iii)由框图中数据计算,可得石英管A左侧固体中铁元素的百分含量为。
(本题14分)某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中加入l—2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe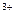 、Br2谁的氧化性更强?
、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe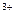 >Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含(填化学式,下同)所致。
>Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含(填化学式,下同)所致。
②乙同学认为氧化性:Fe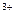 <Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含所致。
<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含所致。
(3)设计实验并验证
丙同学为验证乙同学的观点。选用下列某些试剂设计两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a、酚酞试液 b、四氯化碳 c、无水酒精 d、硫 氰化钾溶液
氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂(填序号) |
实验现象 |
|
| 方案1 |
||
| 方案2 |
(4)结论
氧化性:Fe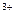 <Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为。
<Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为。
(5)实验后的思考
在2molFeBr2溶液中通入一定量的Cl2,当有33.6L Cl2(标准状况)与FeBr2溶液发生了反应,所发生反应的离子反应方程式为。
某学生设计如下实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题: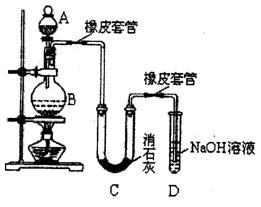
(1)A仪器的名称是,所盛试剂是。
(2)漂白粉将在U型管中产生,其化学反应方程式是。
(3)有同学建议在两个橡皮套管内的两段玻璃导管管口应尽量紧靠,原因是。
(4)此实验所得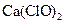 产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了氯酸钙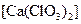 ,为避免此副反应的发生,可采取的措施是;
,为避免此副反应的发生,可采取的措施是;
②试判断另一个副反应是(写出此反应方程式)。
为避免此副反应发生,可采取的措施是。
化学是一门以实验为基础的自然学科,进化化学实验时要采取正确的实验操作,注意实验安全。
(1) 在盛放浓硫酸的试剂瓶的标签上印有如图所示的警示标志,说明浓硫酸是一种。
在盛放浓硫酸的试剂瓶的标签上印有如图所示的警示标志,说明浓硫酸是一种。
(2)下列实验能达到目的的是。
| A.在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸 |
| B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜加快反应速率 |
| C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D.加入盐酸以除去硫酸钠中的少量碳酸杂质 |
E.制取Fe(OH)2时,吸取除去氧气NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再注入NaOH溶液
(3)某化学小组设计如图装置完成一组实验: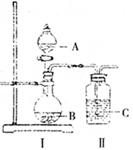
A中装硝酸,B中装石灰石,C中装漂白粉溶液,现象是装置II中产生白色沉淀。他得出酸性:HNO3>H2CO3>HClO。由此得出元素非金属:N>C>Cl。你认为他得出的结论是否正确?答:(填“正确”或“不正确”)。理由是。
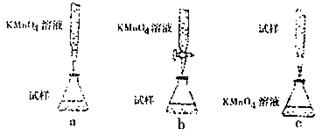
(4)有些同 学认为用KMnO4溶液滴定也能进行铁元素含量的测定(5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O)
学认为用KMnO4溶液滴定也能进行铁元素含量的测定(5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需。
②该实验中的KMnO4溶液需要酸化,用于酸化的酸是。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③某同学设计的下列滴定方式,最合理的是(夹持部分略去)(填字母序号)