下表是摘自国家环境监测中心公布的某时间我国部分大城市空气的监测周报.
| 城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
| 北京 |
92 |
TSP |
Ⅱ |
济南 |
76 |
TSP |
Ⅱ |
| 天津 |
82 |
TSP |
Ⅱ |
武汉 |
83 |
NOx |
Ⅱ |
| 长春 |
103 |
TSP |
Ⅲ |
深圳 |
77 |
NOx |
Ⅱ |
| 上海 |
74 |
NOx |
Ⅱ |
汕头 |
54 |
|
Ⅱ |
| 杭州 |
67 |
TSP |
Ⅱ |
成都 |
87 |
TSP |
Ⅱ |
| 福州 |
42 |
|
Ⅰ |
重庆 |
98 |
SO2 |
Ⅱ |
| 厦门 |
25 |
|
Ⅰ |
贵阳 |
69 |
TSP |
Ⅱ |
注:TSP:空气中飘尘;NOx:含氮氧化物.
阅读分析上表,回答下列问题:
(1)经济特区中,空气质量最好的城市是________,直辖市中空气质量最差的城市是________.
(2)最容易出现酸雨的城市是________.为防止城市出现酸雨,降低煤燃烧时向大气排放的SO2,工业 上将生石灰或石灰石和含硫煤混合使用.请写出燃烧时,有关“固硫”(不使含硫化合物进入大气)反应的化学方程式________________________________________________________________.
已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,甲是中学化学中常见的红棕色粉末状固体,它们之间的相互转化关系如图所示(部分产物及反应条件没有列出):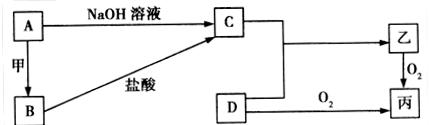
(1)写出框图中A转化为B的化学方程式:_______________________________________,该反应属于______________(填“吸热反应”或“放热反应”)。
(2)若乙的水溶液呈弱酸性,丙是一种大气污染物、有刺激性气味。已知16 g固体单质D完全燃烧转化成丙时,放出148.4 kJ的热量,则该反应的热化学方程式为:
_____________________________________________________________________________。
(3)若乙在水溶液中呈弱碱性,其盐可用作化肥,且C与D化合生成乙的反应是可逆反应。
①将等物质的量的C、D两种单质充入一体积恒定的密闭容器中,在适当催化剂和恒温条件下反应,下列说法中不正确的是____________(填字母)。
a.达到化学平衡时,2υ正(C) = 3υ逆(乙)
b.反应过程中,D单质的体积分数始终为50%
c.达到化学平衡时,混合气体的密度保持不变
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡后,再升高温度,乙的体积分数增大
②若在一个体积为10 L的密闭容器中,充入8 mol C单质和2 mol D单质,在一定温度下发生反应生成气体乙,经40 min后反应达到平衡,此时C的转化率为37.5%。从反应开始到达平衡的40 min内,用物质乙表示的化学反应速率为_________________________;达到平衡后,若向容器中按5∶1∶2的物质的量之比再次充入C、D、乙三种物质,则原平衡体系中C的转化率将_____________(填“增大”、“减小”或“不变”)。
某有机物蒸汽对H2的相对密度为43,请根据以下信息回答相应的问题:
(1)若该有机物A属于烃类,则分子式为_______________;写出其同分异构体中,一溴代物有3种物质的结构简式并命名:
____________________________________________________________________________。
(2)若该有机物B分子中C、H、O的原子个数之比为2∶3∶1,B物在酸性条件下水解可生成碳原子数相同的两种有机物C和D,B通过加聚反应可制得有机高分子化合物M,M常用做木材的黏合剂,俗称“乳白胶”。
①B分子中不含氧的官能团的名称为_________________________;
②B的同分异构体中属于链状不饱和羧酸的有三种,它们的结构简式是:
_________________________、_______________________、_________________________;
③写出B在一定条件下加聚反应生成M的化学方程式:
_____________________________________________________________________________;
④通常羟基与双键碳原子直接相连时,易发生下列转化: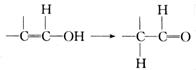
D能发生银镜反应,请写出D的结构简式:______________________________;
⑤已知:
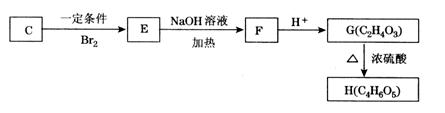
C可以发生如上图所示转化关系,写出以下化学方程式:
E→F:__________________________________________________________________;
G→H:__________________________________________________________________。
短周期主族元素A、B、C、D原子序数依次增大,且只有C为金属元素。A、C位于同一主族,B是地壳中含量最多的元素,B、C的最外层电子数之和与D的最外层电子数相等。请回答下列问题:
(1)D的最高价氧化物的水化物的名称为__________________。
(2)C2B2的电子式为_________________________,其中含有的化学键类型为
_________________。
(3)由上述四种元素中的三种组成某种盐,水溶液显碱性,是家用消毒剂的主要成分。将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为:
________________________________________________________________________。
(4)用石墨电极电解CD的饱和溶液,电解反应的离子方程式为:________________________________________,若反应后溶液的体积为200 mL,测得pH为13(常温下测定),则阳极得到的气体质量为_______________,外电路中通过电子的物质的量为___________________。
(5)实验室欲检验CD溶液中所含的D–,操作方法和现象为_____________________________________。
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: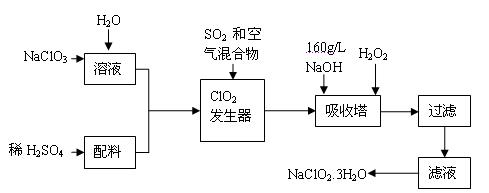
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2 3H2O。
3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③HClO2可看成是强酸。
(1)160 g/L NaOH溶液的物质的量浓度为 。若要计算该溶液的质量分数,还需要的一个量是 (用文字说明)。
(2)发生器中鼓入二氧化硫的作用可能是 (填序号)。
A.将SO2氧化成SO3,增强酸性 B.稀释ClO2以防止爆炸;
C.将NaClO3还原成ClO2
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是。
(4)吸收塔内的反应的化学方程式为 。吸收塔的温度不能超过20℃,其目的是防止H2O2分解,写出H2O2分解的化学方程式:。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (填序号)。
A.Na2S B.Na2O2C.FeCl2
(6)从滤液中得到NaClO2 3H2O粗晶体的实验操作依次是 (填序号)。
3H2O粗晶体的实验操作依次是 (填序号)。
A.蒸发 B.蒸馏 C.冷却结晶 D.灼烧 E.过滤
要得到更纯的NaClO2 3H2O晶体能否加热蒸干 (填“能”或“不能”)。
3H2O晶体能否加热蒸干 (填“能”或“不能”)。
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取一般可以通过下列两个反应完成:
反应①: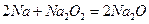
反应②: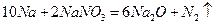
(1)分析以上两个反应,完成下表:
| 作氧化剂的元素(填元素符号) |
基本反应类型 |
|
| 反应① |
||
| 反应② |
置换反应 |
(2)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,上述两个反应中满足“原子经济”要求的是(填序号)
(3)欲将23g钠全部转化成Na2O,现按照反应:①进行反应,需先将一部分钠氧化成Na2O2,则被氧化成Na2O2的金属钠的物质的量为。
(4)Na2O在空气中很容易进一步氧化成Na2O2。100g某Na2O样品(含Na2O2)中加入足量的水,生成5.6L气体(标准状况),则样品中Na2O的质量分数为。