(12分)某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:
(1)放电时,正极的电极反应式为 ;充电时,Pb电极应该连接在外接电源的 (填“正极”或“负极”)。
(2)工业用PbO2来制备KClO4的工业流程如下: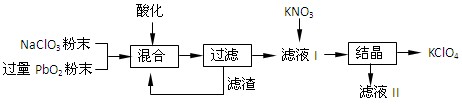
①写出NaClO3与PbO2反应的离子方程式: 。
②工业上可以利用滤液Ⅰ与KNO3发生反应制备KClO4的原因是 。
(3)PbO2会随温度升高逐步分解,称取23.9gPbO2,其受热分解过程中各物质的质量随温度的变化如右图所示。
若在某温度下测得剩余固体的质量为22.94g,则该温度下PbO2分解所得固体产物的组成为 (写化学式),其物质的量之比为 。
氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
① 工业合成氨的热化学方程式是。
② 若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则
Q(填“>”、“<”或“=”)_______184.4 kJ。
③ 已知:
1 mol N-H键断裂吸收的能量约等于_______kJ。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
| T / ℃ |
165 |
175 |
185 |
195 |
| K |
111.9 |
74.1 |
50.6 |
34.8 |
①焓变ΔH(填“>”、“<”或“=”)0
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)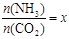 ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是。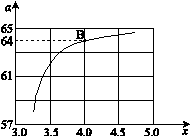
③ 上图中的B点处,NH3的平衡转化率为_______。
(3)氮气是制备含氮化合物的一种重要物质,而氮的化合物用途广泛。
下面是利用氮气制备含氮化合物的一种途径:
①过程Ⅱ的化学方程式是
②运输时,严禁NH3与卤素(如Cl2)混装运输。若二者接触时剧烈反应产生白烟,并且0.4 mol NH3参加反应时有0.3 mol 电子转移。写出反应的化学方程式
③氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。
已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g) ΔH =" ―1316" kJ/mol,则该燃料电池的负极反应式是。
X、Y、Z、L、M、N六种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是短周期原子半径最大的元素,N是地壳中含量最高的金属元素。
用化学用语回答下列问题:
(1) M在元素周期表中的位置为;六种元素的原子半径从大到小的顺序是
(2)Z、X两元素按原子数目比l∶3构成分子A, A的电子式为,Y、L两元素按原子数目比l∶2构成分子B,B中所含的化学键类型为。
(3)硒(se)是人体必需的微量元素,已知非金属性:34Se<L。请结合原子结构解释原因。
(4)用Y、L、M构成的正盐溶液可以清除油污,请结合离子方程式以及必要的文字解释原因。
(5)用石墨作电极,NCl3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出电解熔融Q制取N的电极方程式:阳极:;阴极:。
已知:化合物F是用于制备药品盐酸祛炎痛的中间产物,其合成路线为: 
已知:(Ⅰ)RNH2+R/CH2Cl  RNHCH2 R/+HCl(R和R/代表烃基)
RNHCH2 R/+HCl(R和R/代表烃基)
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ) (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)
(Ⅳ) 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
回答下列问题:
(1)D中含有的官能团名称为;E含有的官能团名称为、
(2)反应①~⑤中,属于取代反应的是(填反应序号)
(3)检验D中官能团的实验操作如下:取少量D于试管中,
(4)C的结构简式是
(5)D+E→F的化学方程式:
(6)已知E的一种同分异构体(对位氨基)在一定条件下,可聚合成热固性很好的高分子,写出合成此高聚物的化学方程式:
(7)已知某有机物M的分子式为C9H11Cl,符合下列条件的M的同分异构体有种。①与D互为同系物
②M为二取代苯化合物。
PBS是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:
(已知: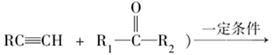
 )
)
(1)A→B的反应类型是________;B的结构简式是________________。
(2)C中含有的官能团名称是________;D的名称(系统命名)是________________。
(3)半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和1个羟基,但不含—O—O—键。半方酸的结构简式是________________。
(4)由B和D合成PBS的化学方程式是______________。
(5)下列关于A的说法正确的是________。
a.能使酸性KMnO4溶液或溴的CCl4溶液褪色
b.能与Na2CO3反应,但不与HBr反应
c.能与新制Cu(OH)2反应
d.1 mol A完全燃烧消耗5 mol O2
萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成α萜品醇G的路线之一如下:
已知:RCOOC2H5

请回答下列问题:
(1)A所含官能团的名称是________。
(2)A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式:________________。
(3)B的分子式为________;写出同时满足下列条件的B的链状同分异构体的结构简式:________________。
①核磁共振氢谱有2个吸收峰
②能发生银镜反应
(4)B→C、E→F的反应类型分别为________、________。
(5)C→D的化学方程式为______________________________________。
(6)试剂Y的结构简式为________________。
(7)通过常温下的反应,区别E、F和G的试剂是________和________。
(8)G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式:________________。