(共15分)下图每一方框中的字母代表一种反应物或生成物。产物J是含金属元素A的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体。试填写下列空白: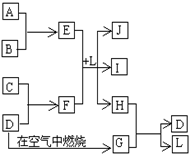
(1)框图中所列物质中属于非电解质的物质名称为 ;
(2)用电子式表示出H的形成过程 ;
(3)将E的水溶液蒸干并灼烧得到的固体物质的化学式为 ;
(4)F的水溶液中各离子浓度由大到小的顺序为 ;
(5)F的水溶液显碱性的原因:(用离子方程式表示) ;
(6)E与F在L中反应的离子方程式为 ;
(7)H和G之间反应的化学方程式为 .
(2分) 书写下列微粒的电子式:
⑴CS2;⑵Ca(OH)2 。
有下列各组物质:
| A.O2和O3(臭氧) | B. |
C.CH3CH2CH2CH3和 |
D. |
E.葡萄糖和果糖 F.(CH3)2CH2与C(CH3)4
G.淀粉和纤维素 H.液氯与氯气
(1)组两物质互为同位素(2)组两物质互为同素异形体
(3)组两物质属于同系物(4)组两组物质互为同分异构体
(5)组中的物质是同一物质
(3分)下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
(1)图中属于烷烃的是(填编号)属于烯烃的是,(填编号)
(2)上图中与B互为同分异构体但不属于同种类的物质的是:。(填编号)
(6分)已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
请回答下列问题:(1)写出A的结构简式。
(2)物质B可以被直接氧化为D,需要加入的试剂是。
(3)写出下列反应的化学方程式:
①;反应类型:。
④。反应类型:。
如图所示装置:
①若烧杯中溶液为稀硫酸,
电极反应式为:正极;
负极。
②若烧杯中溶液为氢氧化钠溶液,则负极为,
总反应方程为。