(本题共13分)
有机物A1和A2分别和浓H2SO4在一定温度下共热都生成烃B,B的蒸气密度是同温同压下H2密度的59倍,在催化剂存在下,1mol B可以和4mol H2发生加成反应,B的一元硝化产物有三种(同种类型)。有关物质之间的转化关系如下:([O]表示氧化反应)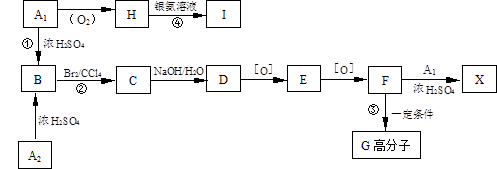
52、反应①属于 反应,反应②属于 反应
53、写出A2和X两种物质的结构简式:
A2 X
54、书写化学方程式:
③
④
55、化合物E有多种同分异构体,请写出其中属于酯类且具有两个对位侧链的同分异构体的结构简式:
已知溴乙烷跟氰化钠(NaCN)反应后再水解可以得到丙酸:
CH3CH2Br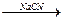 CH3CH2CN
CH3CH2CN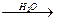 CH3CH2COOH
CH3CH2COOH
产物分子比原化合物分子多了一个碳原子,增长了碳链,请根据以下框图完成问题: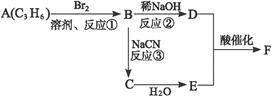
(F分子中含有8个原子组成的环状结构)
(1)反应①②③中属于取代反应的是____________(填反应代号)。
(2)写出结构简式:E.__________________________,F.___________________________。
酚酞是常用的酸碱指示剂,结构简式为: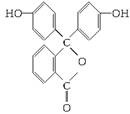
(1)酚酞的分子式为______________________________。
(2)酚酞属于_____________________、________________类衍生物。
(3)酚酞分别在1 mol·L-1 HCl和1 mol·L-1 NaOH溶液中溶解,在_____________中的溶解度大,原因是_________________________________________________________________。
某化工厂的废液经测定得知主要含有乙醇,其中还溶有苯酚(熔点:43 ℃)、乙酸和少量二氯甲烷。现欲从废液中回收它们,根据各物质的熔点和沸点,该工厂设计了以下回收的实验方案。
请完成下列问题:
(1)写出试剂A____________、B____________、C____________的化学式:A____________,B____________,C____________;
(2)写出操作D的名称:D________________;
(3)写出回收物①②和G的组成:①______________,②____________,G____________。
已知:
乙烯酮与活泼的氢化物易发生加成反应,如与HCl的反应如下:
从乙酸出发,可发生下图转化:
完成下列问题:
(1)上面乙酸转化图中,将每种类型反应的个数填入空格,取代反应_____________个,加成反应_____________个,消去反应_____________个。
(2)C的结构简式为_______________________,D的结构简式为____________________。
(3)C的同分异构体甚多,其中含1个—OH和四元环(由3个C、一个O构成)的环酯类化合物有_____________种。
(4)写出A D的化学方程式_______________________________________________。
D的化学方程式_______________________________________________。
分子式为C3H6O3的物质有多种同分异构体,请写出符合下列要求的各种同分异构体的结构简式。说明:①不考虑同一碳原子上连两个羟基;②乙炔、苯等分子中同类原子化学环境相同,丙烷、丁烷等分子中同类原子化学环境有两种。
(1)甲分子中没有甲基,且1 mol甲与足量金属Na反应生成1 mol H2。若甲还能与NaHCO3溶液反应,则甲的结构简式为__________________________;若甲还能发生银镜反应,则甲的结构简式为_________________________。
(2)乙分子中所有同类原子的化学环境相同,且不与金属Na反应,则乙结构简式为:_______。
(3)丙分子中碳与氧分别有两种化学环境,氢的化学环境相同,且丙与金属Na不反应,则丙结构简式为__________________________________________。