请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)我国储氢纳米碳管研究已取得重大进展。用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
___C + ___K2Cr2O7 + _______=" ___" CO2↑ + ___K2SO4 + ___Cr2(SO4)3 +___H2O
请完成并配平上述化学方程式。
(2)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g)  CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1
①下列措施中有利于增大该反应的反应速率的是____________。
| A.使用高效催化剂 | B.降低反应温度 |
| C.增大体系压强 | D.不断将CH3OH从反应混合物中分离出来 |
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2)/n(CO)的起始组成比的关系如右图所示。已知容器体积1L,起始时CO的物质的量均为1mol。据此判断在上述三种温度中,曲线Z对应的温度是__________;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K =_______________________。
③已知: △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1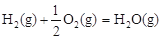 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气的热化学方程式为_________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其溶度积常数Ksp=c(Ca2+)·c(CO32—)=2.8×10−9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10 -5 mol/L ,则生成沉淀所需CaCl2溶液的最小浓度为________________________。
为实现以下各步的转化,请在括号内填入适当试剂的化学式
已知有四种有机物A、B、C、D,其分子式均为C3H6O2,分子结构中均有甲基把它们分别进行实验并记录现象如下:
| 有机物 |
氢氧化钠 |
银氨溶液 |
新制氢氧化铜 |
金属钠 |
| A |
发生中和反应 |
不反应 |
溶解 |
放出氢气 |
| B |
不反应 |
发生银镜反应 |
生成红色沉淀 |
放出氢气 |
| C |
发生水解反应 |
发生银镜反应 |
生成红色沉淀 |
不反应 |
| D |
发生水解反应 |
不反应 |
不反应 |
不反应 |
则A、B的结构简式为:A________;B________;C、D的名称:C__________;D________
在一定温度下,在10L密闭容器中加入5molSO2和一定量的氧气,在一定条件下发生反应: 2SO2(g)+O2(g) 2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
(1)氧气的起始浓度为。
(2)平衡时剩余SO2mol;
(3)该条件下SO2的最大转化率为;
(4)平衡时体系中SO3的百分含量(体积分数)为 ;
(5)平衡体系中SO2、O2和SO3的物质的量之比为。
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要吸收能量,形成化学键要放出能量。已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。则由氢气和碘单质反应(H2+I2=2HI)生成1 mol HI需要(填“放出”或“吸收”)___kJ的热量。
(2)在生产和生活中经常遇到化学能与电能的相互转化。
在如图甲装置中,负极电极反应式为,发生的是反应(填“氧化”或“还原”,下同)。正极电极反应式为;总反应的离子方程式为。
(3)若用氢氧化钾溶液做电解质溶液,用氢气做燃料,空气做氧化剂制成燃料电池,其负极反应式为;正极反应式为。当有标状下2.24L氢气消耗时,另一极消耗氧气的物质的量为。
(4)在如下图所示的原电池中,铝做极,导线上电子由极流向极。
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为;
(2)从开始至2min,Z的平均反应速率为;
(3)3min时,混合物中X的物质的量浓度为。
(4)2分钟后X、Y、Z各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了状态。
(5)下列叙述能说明上述反应达到平衡状态的是(填序号)
A.X、Y、Z的物质的量之比为1∶2∶3 |
B.混合气体的压强不随时间的变化而变化 |
C.单位时间内每消耗3 mol X,同时生成2 mol Z |
D.混合气体的总质量不随时间的变化而变化 |
 E.混合气体的总物质的量不随时间的变化而变化
E.混合气体的总物质的量不随时间的变化而变化
F.混合气体的平均相对分子质量不再随时间的变化而变化
G.混合气体的密度不再随时间的变化而变化
H.2υ正(X)= 3υ逆(Z)