下列叙述正确的是
A.在0.10 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO ) ) |
| B.甲烷的标准燃烧热是890.3 kJ·mol-1,则甲烷燃烧的热化学方程式是: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1 |
| C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 电解 2Cu+O2↑+4H+ |
| D.以KOH为电解质溶液的甲醇燃料电池的负极电极反应式: |
CH3OH-6e-+H2O=CO2↑+6H+
某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程: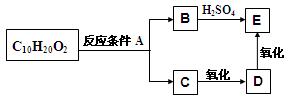
则符合上述条件的酯的结构可有
| A.2种 | B.4种 | C.6种 | D.8种 |
下列离子方程式正确的是
A.乙酸与碳酸钠溶液反应:2H++CO == CO2↑+H2O == CO2↑+H2O |
| B.醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2—→Cu2++2H2O |
| C.苯酚钠溶液中通入少量二氧化碳: 2C6H5O-+CO2+H2O  2C6H5O 2C6H5O H+CO H+CO |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+4[Ag(NH3)2]++4OH- CO
CO +2NH
+2NH +4Ag↓+6NH3+2H2O
+4Ag↓+6NH3+2H2O
黄曲霉素的结构如图,1 mol该化合物分别与H2、NaOH溶液反应,最多消耗H2和 NaOH分别为
| A.6 mol 2 mol | B.7 mol 2 mol |
| C.6 mol 1 mol | D.7 mol 1 mol |
可以将六种无色液体:C2H5OH、AgNO3溶液,C2H5Br、KI溶液,C6H5OH溶液,C6H6一一区分开的试剂是
| A.HCl溶液 | B.溴水 | C.酸性KMnO4溶液 | D.NaOH溶液 |
下列叙述正确的是
| A.淀粉、纤维素、油脂都属于高分子化合物 |
| B.能发生酯化反应的酸一定都是羧酸 |
| C.淀粉与纤维素互为同分异构体 |
| D.油脂水解得到的醇是丙三醇 |