下列化学用语中表达正确的是
A.四氯化碳的电子式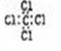 |
B.C2 H4的结构简式:CH2CH2 |
C.环已烷的结构简 |
D.次氯酸的结构式:H-Cl-O |
下列各组有机物,不论按何种比例混合,只要总质量一定,完全燃烧生成水的总质量就相同的是()
| A.甲烷、丙烷 | B.甲苯、甘油 | C.甲酸、乙酸 | D.乙醇、乙二醇 |
下列实验装置图完全正确的是()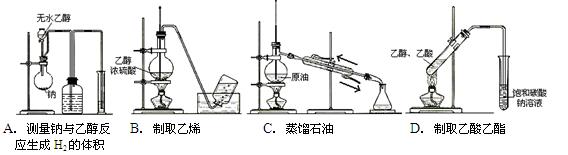
提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是()
| 被提纯的物质 |
除杂试剂 |
分离方法 |
|
| A |
乙酸乙酯(乙酸) |
CCl4 |
萃取、分液 |
| B |
乙烷(乙烯) |
酸性KMnO4溶液 |
洗气 |
| C |
溴苯(溴) |
氢氧化钠溶液 |
分液 |
| D |
苯(苯酚) |
浓溴水 |
过滤 |
下列说法中正确的是()
| A.卤代烃在NaOH存在下水解生成的有机物都是醇 |
| B.所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
C.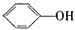 与 与 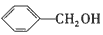 互为同系物 互为同系物 |
| D.分子式为C3H8与C6H14的两种有机物一定互为同系物 |
要鉴别己烯中是否混有少量甲苯,正确的实验方法是()
| A.先加足量溴水,然后再加入酸性高锰酸钾溶液 |
| B.先加足量的酸性高锰酸钾溶液,然后再加入溴水 |
| C.点燃这种液体,然后再观察火焰的颜色 |
| D.加入浓硝酸后加热 |