某化学反应2A(g)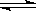 B(g)+D(g)在四种不同条件下进行,反应器均为相同的恒容密闭容器,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,反应器均为相同的恒容密闭容器,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表: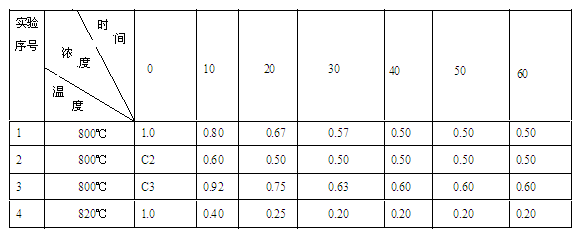
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内用A表示的平均速率为 ;
(2)在实验2,A的初始浓度C2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 ;
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、<=),且C3= mol/L。
23实验室有一瓶碳酸钠试剂,含有少量的硫酸钠杂质,某学生设计以下实验来确定其纯度。
| A.称取样品W1 g | B.加盐酸酸化 | C.用蒸馏水溶解 | D.过滤 |
E.加入过量的氯化钡溶液 F.洗涤沉淀 G.干燥沉淀 H.称量沉淀的质量W2 g
(2)酸化时盐酸必须过量,其目的是______。
(3)氯化钡溶液要过量的目的是______。检验氯化钡过量的方法是______。
(4)检验沉淀已洗涤干净的方法是______。
(5)样品中碳酸钠的纯度为______。
请利用下列装置及试剂组装一套装置。其流程是,用浓盐酸和MnO2先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答: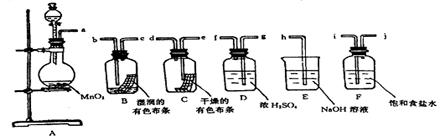
(1)按气体从左向右流向将各装置依次连接起来(填接口标号):
a接,接,接,接,接 h。
装置中存在什么问题。
(2)烧瓶中发生反应的化学反应方程式是。
(3)D装置的作用是,F装置的作用是。
(4)C瓶中的现象是,以上事实说明起漂白作用的物质是。
(5)E中反应的离子方程式是。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe的氧化物和SiO2,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下: 
试回答下列问题:
(1)B物质的化学式是在未加入H2O2的溶液中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是(填代号)。
| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
(2)向溶液A加入H2O2的作用是剂(填氧化或还原),离子反应方程式为,选用H2O2而不用Cl2的原因是。
(3)由溶液C获得CuSO4·5H2O,需要经过,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是。
(4)制备CaCO3时,先通入(填NH3或CO2),若实验过程中有氨气逸出,可选用下列装置中的 (填代号)装置吸收氨气。(烧杯中的液体都为水)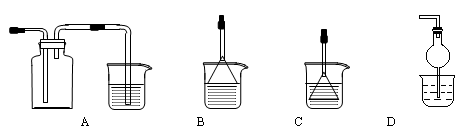
(12分)手持技术又称掌上技术,是由数据采集器、传感器和配套的软件成
的定量采集各种常见数据并能与计算机连接的实验技术系统。某研究小组利用手持技术,获得8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
(1)试确定78℃时固体物质M的化学式:。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成且两种气体的组成元素相同,摩尔质量相差16,写出该反应的化学方程式。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
①试剂X的名称是。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c。
③充分反应后,利用装置Ⅲ中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次 称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量为(填计算式)。
④上述测得P的质量比实际分解质量要小,原因是。
(14分)(1)向1 L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为,AlCl3的物质的量。
(2)已知:2Fe3++2I- = 2Fe2++ I2; 2Fe2++Br2= 2Fe3++2Br-
①向含有1mol FeI2和1.5mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是 。
②如果向①的溶液中通入3mol Cl2,则被氧化的离子对应的氧化产物分别是 。
(3)①若m g铁屑与含有 n gHNO3的硝酸溶液恰好完全反应,若 m : n =" 1" : 2.7,该反应的化学方程式为 __________________________________________________(假设还原产物只有一种,且只生成一种盐)
②若含 n g HNO3的稀硝酸溶液恰好使5.6g铁粉完全溶解,若有 n/4 gHNO3被还原成NO(无其它还原产物)则 n 的范围为_________________________
③某条件下锌和硝酸反应时的物质的量之比为2:5,此时硝酸的还原产物是____________