[化学——选修2:化学与技术](15分)
碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本。
(1)写出化学气相沉积法制造金刚石薄膜的化学反应方程式: ;
(2)化学方法制备高纯度的单质硅工艺涉及到的的主要方程式(3个)为 ; ; 。
(3)最近科学家提出一种“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为甲醇。其技术流程如下: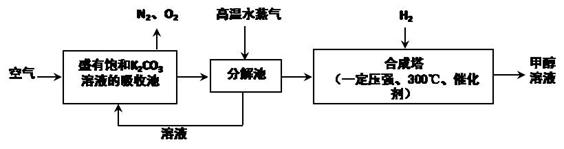
①碳酸钾溶液所起的作用是 ;
②写出上述流程中分解池中发生反应的化学方程式 ;
③在合成塔中,若有2.2 kg CO2与足量H2恰好完全反应,生成气态的水、甲醇,可放出2473.5 kJ的热量,试写出合成塔中发生反应的热化学方程式 ;
④“绿色自由”构想技术流程中常包括物质和能量的循环利用,上述流程中能体现循环利用的物质有 。
如图所示,甲、乙、丙是三种常见单质,X、Y、Z是常见化合物,它们之间有如下转化关系:
⑴若甲是短周期金属单质,乙、丙是短周期非金属单质,X、Y、Z中只有一种是离子晶体,
试推断:
①X的电子式是______________________________。
②X与甲反应的化学方程式____________________________________。
⑵若甲是气体单质,丙通常是液体,Y和Z具有相同的阳离子,X与Z含有相同的阴离子,试推断:
①写出Z的化学式_______________________。
②写出X与足量的甲在溶液中完全反应的离子方程式:_________________________ 。
(1)用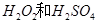 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知: ====
==== △H=+64kJ/mol
△H=+64kJ/mol ====
====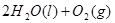 △H= -196kJ/mol
△H= -196kJ/mol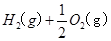 ="==="
="==="  △H= -286kJ/mol
△H= -286kJ/mol
在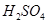 溶液中
溶液中 与
与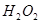 反应生成
反应生成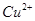 和
和 的热化学方程式为 。
的热化学方程式为 。
(2)控制其他条件相同,印刷电路板的金属粉末用10℅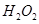 和3.0 mol/L的
和3.0 mol/L的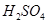 混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
| 温度(℃) |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
| 铜平均溶解速率 |
7.34 |
8.01 |
9.25 |
7.98 |
7.24 |
6.73 |
5.76 |
|
(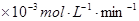 ) ) |
||||||||
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
(3)在提纯后的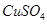 溶液中加入一定量的
溶液中加入一定量的 和
和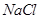 溶液,加热,生成
溶液,加热,生成 沉淀。制备
沉淀。制备 的离子方程式是 。
的离子方程式是 。
(6分)某课外活动小组同学用如图装置进行实验,试回答下列问题。
(1)若开始时开关K与b连接,则B极的电极反应式为。
总反应的离子方程式为。
有关上述实验,下列说法正确的是(填序号)。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质相同的状态(质量和浓度均相同)
④若标准状况下B极产生2.24 L气体,则电路中转移0.2 mol电子
(2)若开始时开关K与a连接,则B极的电极反应式为
。
15.6 g Na2X含Na+ 0.4mol,则Na2X的摩尔质量为,X的相对原子质量为 。
写出下列物质在水中的电离方程式:
(1)硫酸钠
(2)氢氧化钡