(4分) 探究小组用滴定法测定CuSO4·5H2O(Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol ·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++H2Y2-===CuY2-+2H+
(1)写出计算CuSO4·5H2O质量分数的表达式w=_______________;
(2)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是________。
A.未干燥锥形瓶 B.滴定终点时滴定管尖嘴中产生气泡
C.未除净可与EDTA反应的干扰离子
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的最高价氧化物对应的水化物的化学式为H2XO3 |
| Y |
Y是地壳中含量最高的元素 |
| Z |
Z元素的最外层电子数与电子层数相同 |
| W |
W的一种核素的质量数为28,中子数为14 |
(1) W位于元素周期表第周期第族;Z的离子结构示意图:_____________
四种元素的原子半径从大到小的顺序为:__________________________(用元素符号表示)
(2)氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称。
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是_____________
W的最高价含氧酸钠盐显_____性(填“酸”、“碱”或“中”),其用途是__________________
(4)常温下,不能与z单质发生反应的是_________(填序号)
a.CuSO4溶液 b.Fe2O3c.浓硫酸 d.NaOH e.Na2CO3固体
在25°、101kPa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,Z的燃烧热的热化学方程式是_________________________________。
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为、 、。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有、。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质的电子式为___________此化合物在酸性条件下与高锰酸钾反应的离子方程式为;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为。
加碘食盐中通常加入的是KIO3,该物质在酸性条件下表现出较强的氧化性,可以和碘化物、亚硫酸盐等还原性物质发生反应。
(1)写出KIO3与KI在稀硫酸介质中发生反应的离子方程式______________________
(2)为测定菜加碘盐中碘元素的含量,某学生甲设计了如下实验:
A.准确称取wg食盐,使其完全溶解在适量的蒸馏水中;
B.用稀硫酸酸化所得溶液,加入过量的KI溶液,使其充分反应;
C.以___________________为指示剂,运滴加入物质的量浓度为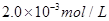 的硫代硫酸钠溶液10.0mL,恰好完全反应,判断反应完全的实验现象为____________________________________,则该加碘盐样品中碘元素的含量为______________________mg/Kg(用含w的代数式表示)。
的硫代硫酸钠溶液10.0mL,恰好完全反应,判断反应完全的实验现象为____________________________________,则该加碘盐样品中碘元素的含量为______________________mg/Kg(用含w的代数式表示)。
(已知: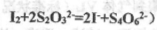 )
)
(3)某学生乙又进行了下列实验:
A.准确称取1.0g纯净的NaCl,加3mL蒸馏水配成溶液,溶液为无色;
B.滴入5滴指示剂和1mL 0.lmol/L Kl溶液,充分振荡,溶液不变化;
C.继续滴加l滴1mol/L的硫酸溶液,充分振荡,溶液变蓝色
推测实验中产生蓝色现象的原因,用离子方程式表示________________________
根据学生乙的实验结果,请对学生甲的实验结果进行分________________________(偏大、偏小、正确),其原因是________________________________________________.
元素周期表是人们研究物质性质的重要工具,下表是元素周期表的一部分,请用化学用语回答下列问题: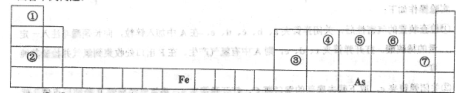
(1)①—⑦号元素原子半径最大的是____,最高价氧化物对应的水化物物酸性最强的是________________.
(2)写出由①-⑦号元素中的几种组成显碱性的盐的化学式____________________。(写出2种即可),并用离子方程式表示其中一种显碱性的原因____________________.
(3)写出③号元素的最高价氧化物与①-⑦号元素中金属性最强的元素的最高价氧化物的水化物反应的离子方程式_____________________。
(4) As在元素周期表中的位置是________________。
(5)As的原子结构示意图为________,其氢化物的电子式为___________.
(6)Y是由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可以与Y的水溶液反应,生成其最高价含氧酸(H3AsO4 ),写出该反应的离子方程式_____________________,
当消耗1mol还原剂时转移电子的物质的量为______________________。
(14分)二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”。工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2。
(1)亚氯酸钠也是一种性能优良的漂白剂,但在强酸性溶液中会发生歧化反应,产生ClO2气体,离子方程式为_________________________________________________。向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为相同pH的硫酸,开始时反应缓慢,稍后一段时间产生气体速率迅速加快。产生气体速率迅速加快的原因是______________________________________。
(2)化学法可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备的ClO2更适合用于饮用水的消毒,其主要原因是___________________________________。
(3)电解法是目前研究最为热门的生产ClO2的方法之一。如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的实验。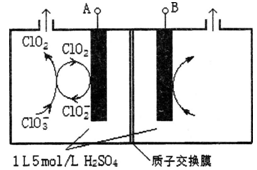
①电源负极为_______极(填A或B):
②写出阴极室发生反应依次为:________________、____________________________;
③控制电解液H+不低于5mol/L,可有效防止因H+浓度降低而导致的ClO2﹣歧化反应。若两极共收集到气体22.4L(体积已折算为标准状况,忽略电解液体积的变化和ClO2气体溶解的部分),此时阳极室与阴极室c(H+)之差为______________。