A、B、C、D 四种主族元素原子序数均在20以内,A元素所处的周期数、主族序数、原子序数均相等,B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3 ,C元素原子的最高正价为+6价,C的阴离子与D的阳离子具有相同的电子排布,D可与C形成化合物D2C。
(1)D元素的名称_______;B在周期表中的位置:第_______周期第_______族
(2)A、B形成的化合物以_______共价键相结合(填极性或非极性)
(3)以C的最高价氧化物对应的水化物作为电解质溶液,组成氢氧燃料电池,放电时则负极区溶液的pH_______(填增大、减小、不变)
(4)以D的最高价氧化物对应的水化物作为电解质溶液,组成氢氧燃料电池,则正极的电极反应式为_____________________
(5)A、B、C、D四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示) ____________________________
(6)C的质子数和中子数相等,则C 的原子组成符号为_______它形成的氢化物的还原性_______氯化氢(填强于或弱于)
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。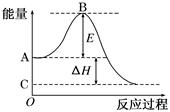
已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
⑴图中A点表示:_____;C点表示:(填“反应物的总能量”“生成物的总能量”)
⑵E的大小对该反应的反应热________(填“有”或“无”)影响。
⑶图中ΔH=________kJ/mol。
已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多。A~H各物质的变化关系如下图所示。
写出各步反应的化学方程式
反应①
反应②
反应③
反应④
反应⑤
按要求完成下列除杂问题
(1)FeCl2溶液中混有少量FeCl3,除杂试剂为,
离子方程式;
(2)FeCl3溶液中混有少量FeCl2,除杂试剂为,
离子方程式;
(3)Fe2O3中混有Al2O3,除杂试剂为,
离子方程式。
(10分)已知A为常见的金属单质,根据下图所示的关系: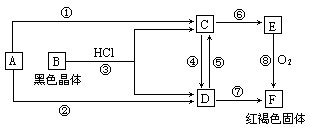
(1)确定A、B的化学式,A为 __________,B为 ___________。
(2)C和D可相互转化,描述C→D溶液的颜色变化:____________________。
④的离子方程式:_____________________________________________________。
⑤的离子方程式:_____________________________________________________。
(3)由E→F的实验现象为:___________________________________。
(6分)实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)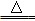 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)写出该反应的离子方程式___________________________________________。
(2)在反应中MnO2发生________(填“氧化”或“还原”)反应,Cl2是________(同上)产物。
(3)当0.1 mol MnO2参加反应时,转移电子数为________,被氧化的HCl为________ mol。