有机物A、B、C、D、E、F、G、H相互转化关系如下图所示。5.2 g F能与100 mL 1 mol/L NaOH溶液恰好完全中和,0.1 mol F还能与足量NaHCO3反应,在标准状况下放出4.48 L CO2。D的分子式为C3H3O2Na,E的分子中含有羧基。
(1)写出物质C中的官能团的名称: ;
(2)写出物质F、H的结构简式;
F 、H ;
(3)写出反应①、④的化学反应类型:① 、④ ;
(4)写出变化①、③的化学方程式;
①
③
(5)写出相对分子质量比B大14,且与B具有相同官能团的所有物质的结构式(不考虑立体异构)。
。
最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”构想技术流程如下: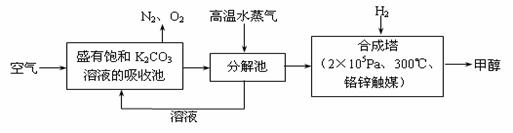
(1)在合成塔中,若有2.2kgCO2与足量H2恰好完全反应,生成气态的水和甲醇,可放出2473.5kJ的热量,试写出合成塔中发生反应的热化学方程式。
(2)①上述合成反应具有一定的可逆性,从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300°C的温度,其原因是。
②“绿色自由”构想技术流程中常包括物质和能量的“循环利用”,上述流程中能体现“循环利用”的除碳酸钾溶液外,还包括。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
| A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1mol CO2和3mol H2 |
(3)甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式。当电子转移的物质的量为时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)常温下,0.1 mol/L KHCO3溶液的pH大于8,则溶液中各种离子浓度由大到小的顺序为:
。
某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
Cl-CO32- NO3- SO42- SiO32- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是(写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是_________________________。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为
_______________________________________________________________
(4)甲同学最终确定原溶液中所含阳离子是,阴离子是。(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为g。
(6)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是
| 选项 |
污染物 |
处理措施 |
方法类别 |
| A |
废酸 |
加生石灰中和 |
物理法 |
| B |
Cu2+等重金属离子 |
加硫酸盐沉降 |
化学法 |
| C |
含复杂有机物的废水 |
通过微生物代谢 |
物理法 |
| D |
碱性的废水 |
用CO2来中和 |
化学法 |
已知88 g D218O 和36 g H216O,请填空:
(1)两者所含的质子数之比为 _______________。
(2)两者所含的中子数之比为 ______ _________ 。
_________ 。
(3)若将它们分别与足量的金属钾反应,则两者产生的气体的质量之比为
A、B、C、D、E为短周期内除稀有气体外的5种元素,它们的原子序数依次增大,其中只有D为金属元 素。B原子的最外层上有4个电子,A和D的最外层电子数相等。D、E两元素原子的质子数之和为A、C两元素质子数之和的3倍。由此可知:
素。B原子的最外层上有4个电子,A和D的最外层电子数相等。D、E两元素原子的质子数之和为A、C两元素质子数之和的3倍。由此可知:
(1)写出元素符号:A为_____,B为_____ ,C为_____,D为______,E为________。
(2)由A和C形成的原子个数比为1:1的化合物的结构式为,
化合物D2C2的电子式为,该化合物中含有的化学键为
(选填离子键、极性键和非极性键)
(3)用电子式表示D2E的形成过程
(4)比较C、D、E的离子半径大小(用离子符号表示)
(5)比较A2C和A2D的沸点、稳定性(用化学式表示)
(6) B的最高价氧化物与D的最高价氧化物反应可得C单质,写出反应的化学方程式
(7) 写出E的最高价氧化物对应水化物的浓溶液与B单质反应的方程式。
按要求完成下列原电池电极反应式或总反应的化学方程式。
(1)负极(Fe);正极(石墨)
电解质溶液(稀硫酸)总反应
(2)负极(Cu); 正极(石墨)
电解质溶液(FeCl3溶液)总反应
(3)用Fe和Cu作电极材料,以浓HNO3为电解质溶液构成的原电池,则负极的电极反应式为;总反应为