同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。他们继续进行了分析、试验和反思:
【查阅资料】
、
等金属氧化物与酸反应,生成盐和水
(1)分析:小燕同学认为一定不是高锰酸钾,原因是
(2)实验一:
| 实验操作 |
||
| ①取一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末溶解,溶液颜色变 |
此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末不溶解,没看到气体产生 |
此粉末一定不是铁粉 |
(3)反思:小华同学认为不做实验①,运用逻辑推理的方法也能得出其中之一是氧化铜的结论,原因是:
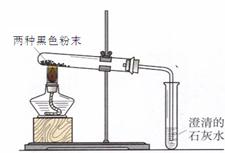
(4)实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变
(7分)某同学设计下表所示实验,探究金属铜对H2O2分解速率的影响。
| 操作 |
装置 |
 现象 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上。 |
 |
|
| 2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中。 |
 |
约1min后可观察到① 和②中都有少量气泡产生 |
| 3、把铜丝插入①中。 |
 |
①中有大量气泡产生,约5min后不再有气泡产生;此时②中 仍然有少量气泡产生 |
回答下列问题:
(1)仪器的①名称是______________,仪器③的名称是______________;
(2)仪器②中实验的目的是;
(3)根据上述实验,可以得出的结论是;
(4)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是________。
A.称量实验前铜丝网的质量
B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰
D.将实验后的铜丝网插入AgNO3溶液中
兴趣小组同学为了弄清即将维修的沼气池中气体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,再用木棍拨动使瓶中的水全部倒出(见右图),然后迅速拉起矿泉水瓶,盖上瓶盖。这种方法属于集气法。
 |
【对气体猜想】
猜想Ⅰ.全部是CH4;猜想Ⅱ.全部是CO;
猜想Ⅲ.全部是CO2;猜想Ⅳ.是CH4和CO2的混合气体。
【实验和推断】
(1)若“现象a”为石灰水变浑浊,则说明气体中含有气体。
(2)步骤②的目的是;步骤③“注水装置”应选右图中的(填序号)。
(3)若“现象b”为杯壁有水雾出现,有同学认为“猜想Ⅰ或Ⅳ”成立,其反应方程式为:
;另有同学认为此现象不能证明收集到的气体中一定含有氢元素,理由是;要排除这种干扰可采取的措施是。
(4)采取(3)中的排除干扰措施后:若“现象a、b”无明显现象,“现象c”石灰水变浑浊,则证明“猜想”成立;若“现象a、c”均为石灰水变浑浊,“现象b”为杯壁有水雾,则证明“猜想”成立。
(12分)现有下列仪器或装置,请回答下列问题:
|
(1)仪器①的名称 ;加热高锰酸钾制取氧气应选装置 (填字母),收集O2应采取 法。
(2)草酸(H2C2O4) 固体在浓硫酸作用下发生反应: H2C2O4======CO2↑+CO↑+H2O,若用该反应来制取CO,制气装置应选 (填字母);除去其中的CO2可选仪器AC,C中装入的试剂最好是 (填小写字母): a. 烧碱溶液 b. 浓硫酸 c. 澄清石灰水。
小青看见爸爸种花时把草木灰洒在花盆中作肥料,她查阅资料得知草木灰的主要成分是一种含钾的化合物。于是她取一些草木灰做了以下实验,请你帮助她将下列实验报告填写完整:
| 实验序号 |
实验目的 |
实验方案 |
实验现象 |
结论 |
| 实验1 |
 |
① ② |
草木灰的主要成分是碳酸钾 |
|
| 实验2 |
探究碳酸钾的性质 |
向碳酸钾溶液中滴入澄清石灰水 |
有白色沉淀生成 |
化学方程式为 |
| 实验3 |
探究实验2反应后上层清液中溶质的成份 |
上层清液中有两种溶质和 |
[反思]实验过程中产生的废液必须处理后再排放。请你对实验2反应后产生的废液处理提出可行的方法。
(6分)超市中的许多食物用保鲜膜包装后出售。保鲜膜为什么可以“保鲜”呢?
[设计实验]在A、B、C三只相同的玻璃杯中,分别注入等体积的蒸馏水,并在各玻璃杯外壁标明刻度,如图所示放置一周。
[实验现象]一周后发现:A杯中的水量几乎不变;而C杯中的水量减少较多;
B杯中的现象是;
[解释]请用分子的知识解释C杯中水量减少的原因:
;
[结论]保鲜膜除了可以阻止食物中水分流失,还能隔绝,防止食物腐败。
[提出新问题]制作保鲜膜的材料是热固性塑料还是热塑性塑料呢?
[实验]在一只试管中放入少量保鲜膜碎片,用酒精灯缓缓加热,观察到碎片熔化,冷却后变成固体,加热又可以熔化。由此得出:制作保鲜膜的材料是(填“热塑性”或“热固性”)塑料。
[反思] (1)保鲜膜虽然能延长食品的保鲜期,但大量使用后丢弃会造成,所以要控制使用。
(2) 化学物质可以造福人类,但有时也会给人类带来危害,请你再举一例说明
。