写出下列反应的化学方程式,并指出反应类型:
(1)实验室制乙烯 ( )
(2)用甲苯制备TNT ( )
(3)苯酚和浓溴水的反应 ( )
(4)1,2-二溴乙烷与其足量氢氧化钠的乙醇溶液加热: ( )
(5)乙醛与银氨溶液的反应 ( )
将太阳能有效地转化为电能是化石燃料耗尽后解决世界能源问题的关键.有人提出以降冰片二烯为介质将太阳能转换为电能的方法:首先让降冰片二烯吸收太阳光转化为其同分异构体四环烷,而后四环烷在催化剂的作用下重新转化为降冰片二烯并放出热量,生成的降冰片二烯循环使用.
(1)降冰片二烯的键线式是 ,其分子式为________.
,其分子式为________.
(2)写出降冰片二烯与H2发生加成反应的化学方程式:________________________________________________________________________.
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫.有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫.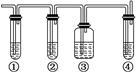
完成下列问题:
(1)图中①、②、③、④装置可盛放的试剂是:
①________;②________;③________;④________.
(将下列有关试剂的序号填入上述空格内)
| A.品红溶液 | B.NaOH溶液 |
| C.浓H2SO4 | D.酸性KMnO4溶液 |
(2)能说明二氧化硫气体存在的现象是__________________________________.
(3)使用装置②的目的是_____________________________________________.
(4)使用装置③的目的是_______________________________________________.
(5)确认含有乙烯的现象是_____________________________________________.
有机化学中有多种同分异构现象,其中有顺反异构,例如2丁烯有两种顺反异构体:A中两个—CH3在双键同侧,称为顺式,B中两个—CH3在双键两侧,称为反式,如下所示: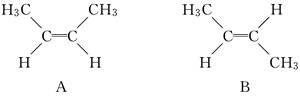
根据此原理,苯丙烯的同分异构体中除有三种位置异构外还有一对顺反异构,写出其结构简式:
(1)三种位置异构:______________,______________,______________;
(2)两种顺反异构: ______________,______________.
乙烯的产量标志着一个国家的石油化工发展水平,它是很重要的工业原料.
(1)已知聚苯乙烯塑料的单体是苯乙烯(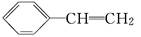 ),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
(2)乙烯的某同系物A(化学式为C5H10)和H2加成后的产物的一氯取代物有3种,试写出A可能有的结构简式:___________________________________________________.
有A、B、C三种有机物,A是一种环状烃,其中碳、氢两种元素的质量比为6∶1,气体A的质量是相同状况下同体积空气质量的1.448倍.B是A的同分异构体,能使酸性高锰酸钾溶液退色.B跟溴水反应生成C.则A、B、C的结构简式分别是________________,__________________,_________________________.