某研究性学习小组为研究铁粉与浓硫酸反应所生成气体的成份并测定各气体的含量,进行了如下实验:【实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体。
(1)该小组作出此推测的理由是: 。
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2 mol/L的H2C2O4标准溶液、0.1 mol/L的酸性KMnO4标准溶液、酸碱指示剂。
b.实验装置设计及组装(加热及夹持装置均已略去)
【实验过程及数据处理】
(2)B中发生反应的离子方程式为: 。
(3)实验前先通入一段时间的N2,其目的是 。
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
。
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25 mL,用H2C2O4标准溶液进行测定。
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平。
( )H2C2O4+( )MnO4- +( )H+ =( )Mn2+ +( ) H2O+( ) ( )
②反应完全的现象是 。
③重复测定两次,平均每次耗用H2C2O4标准溶液15.63 mL,则铁与浓硫酸反应产生的SO2气体
的物质的量为 ;经称量,实验前后装置D的质量减少0.8 g,则产生的气体中SO2的体积分数为 。
实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定CaC2样品的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。
(1)A瓶中的液体可以从酸性KMnO4溶液和FeCl3溶液中选择,应该选择________,它的作用是______________________。
(2)装置Ⅰ的主要缺点是_______________。
(3)装置Ⅱ的主要缺点是____________;若选用此装置来完成实验,则应采取的措施是___________。
(4)若称取a g CaC2,反应完全后,测得B处溴水增重b g,则CaC2的纯度为________。
实验室制乙烯,常常因为温度过高而使乙醇与浓硫酸反应生成少量的二氧化碳,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
(1)写出实验室制取乙烯的化学方程式________________________________
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中可盛放的试剂是:(将下列有关试剂的序号填入空格内)
Ⅰ: 、Ⅱ: 、Ⅲ: 、Ⅳ: 。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
(3)能说明二氧硫存在的现象是 。
(4)使用装置(Ⅱ)的目的是 。
(5)使用装置(Ⅲ)的目的是 。
(6)确证含乙烯的现象 。
(7)进行下列实验时,都要使用温度计,回答下列问题:
制取乙烯时,温度计水银球部位应放在 。
石油分馏时,温度计水银球部位应放在 。
某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:
(2)观察到A中的现象是_______________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是 。
(每空2分,共10分)在试管A中加入3mL乙醇,然后边振荡管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。
(1)试管B中盛放的试剂是 (填名称),实验时往往在B试管中可以看到少量气泡,写出与此现象对应的离子方程式 。
(2)乙醇与乙酸反应的化学方程式是 。
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若要分离B中的液体混合物需要用到的玻璃仪器是 。
(4)用30g乙酸与46g乙醇反应,如果实验产率是理论产率的60%,则可得到的产物质量是 g。
【改编】溴苯是一种常用的化工原料。实验室制备溴苯的实验步骤如下: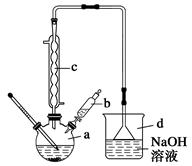
步骤1:在a中加入15 mL苯和少量铁屑,再将b中4.0 mL液溴慢慢加入到a中,充分反应。
步骤2:向a中加入10 mL水,然后过滤除去未反应的铁屑。
步骤3:滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL 水洗涤,分液得粗溴苯。
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品。
(1)步骤1仪器a中发送的主要反应是 。
(2)将d的作用是 。
(3)将b中的液溴慢慢加入到a中,而不能快速加入的原因是 。
(4)仪器c的作用是冷凝回流,回流的主要物质有 。(填化学式)
(5)步骤4得到的粗产品中还含有杂质苯。已知苯、溴苯的有关物理性质如下表,则要进一步提纯粗产品,还必须进行的实验操作名称是 。
| 苯 |
溴 |
溴苯 |
|
| 密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 在水中的溶解度 |
微溶 |
微溶 |
微溶 |