【化学—选修3:物质结构与性质】CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3) 向CuSO4溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。
有以下各组物质,完成以下各组问题:
| A.氧气与臭氧 |
| B.氕与氘 |
C.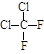 与 与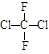 |
| D.乙烯与1-丁烯 |
E.己烷与2,3-二甲基丁烷
(1)以上各组物质属于同系物的是;属于同分异构体的是;属于同素异形体的是;属于同位素的是;属于同一物质的是。
(2)2,3-二甲基丁烷由某烯烃加成得到,则该烯烃的结构简式可能为、。
下图是实验室中制备气体或验 证气体性质的装置图
证气体性质的装置图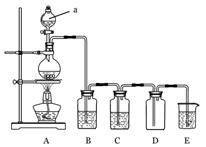
(1)仪器a的名称是_________________。
(2)利用上图装置制备纯净、干燥的氯气。
①圆底烧瓶内发生反应的离子方程式为_______________________________________。
②装置B中的溶液为__________________________;
烧杯中溶液的作用为________________ 。
。
(3)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2。
圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水。
①证明SO2具有漂白性的装置是,现象是
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是
④D装置的作用是。
下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。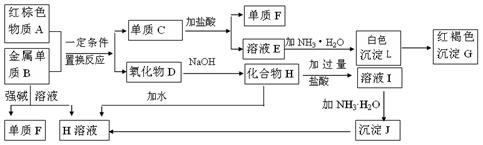
(1)单质B的化学式是,写出物质A的一种用途。
(2)写出单质B与强碱溶液反应的离子方程式,
写出由沉淀J生成 H溶液的离子方程式。
(3)写出白色沉淀L变为红褐色沉淀G的化学反应方程式
。
实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题
(1)制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和。
(2)用托盘天平称取氯化钠固体,其质量为g。
(3)若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________(偏大、偏小或无影响)。
某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等阳离子,阴离子为NO3-,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
待测液中一定含有离子,一定不含有离子,还有一种离子不能确定是否存在,要检验这种离子的实验方法是。