已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数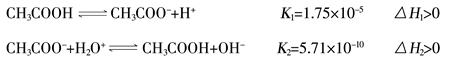
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是
| A.混合溶液PH<7 |
| B.对混合溶液进行微热,K1增大、K2减小 |
| C.调节混合溶液的PH值至中性,则此时溶液中c(Na+)=c(CH3COO—) |
| D.温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO—)减小 |
设NA为阿伏伽德罗常数的值。下列说法正确的是()
| A.3.2g由O2和O3组成的混合物中含有氧原子的数目为0.2NA |
| B.0.1mol苯中含有碳碳双键的数目为0.3 NA |
| C.标准状况下,11.2L三氯甲烷中含有分子的数目为0.5 NA |
| D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4 NA |
下列关于 说法中正确的是()
说法中正确的是()
A. 可用于判断所有条件下的反应能否自发进行 可用于判断所有条件下的反应能否自发进行 |
B. 只用于判断温度、体积一定的反应能否自发进行 只用于判断温度、体积一定的反应能否自发进行 |
C. 只用于判断温度、压强一定的反应能否自发进行 只用于判断温度、压强一定的反应能否自发进行 |
D. <0的反应,在该条件下一定剧烈反应 <0的反应,在该条件下一定剧烈反应 |
下列关于C、Si、Ge、Sn、Pb的比较,正确的是()
A.它们的最外层电子数随核电荷数增加而增多
B.它们的最高价氧化物均可溶于水生成相应的酸
C.它们单质的氧化性随核电荷数的增加而逐渐减弱
D.它们的氢化物的稳定性随核电荷数的增加而逐渐增强
当光束通过下列分散系,能观察到丁达尔现象的是()
①有尘埃的空气②稀盐酸 ③蒸馏水 ④墨水
| A.②③ | B.①④ | C.③④ | D.①②③④ |
俄罗斯科学家用铪和钨两种核素精确确定了地球和月球的年龄,得出月球至少比地球早700万年形成。它们是根据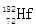 和
和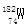 两种核素的含量比例得出的。下列有关
两种核素的含量比例得出的。下列有关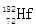 和
和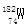 关系的说法正确的是
关系的说法正确的是
| A.中子数相等 | B.原子质量几乎相同 |
| C.互为同位素 | D.在周期表中处于相邻位置 |