下列实验“实验操作”与“结论”对应关系正确的是
| 选项 |
实验操作 |
结论 |
| A |
向Fe(NO3)2溶液的试管中加入稀H2SO4 ,在管口观察到红棕色气体 |
HNO3分解生成了NO2 |
| B |
向沸水中逐滴加入1~2 mL FeCl3饱和溶液,煮沸至红褐色液体 |
制备Fe(OH)3胶体 |
| C |
常温下,向饱和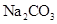 溶液中加少量 溶液中加少量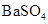 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 |
说明常温下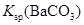 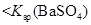 |
| D |
向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
用硫酸酸化的三氧化铬(CrO3)遇酒精后,其颜色由红色变为蓝绿色(反应如下),用此反应可测得司机是否是酒后驾车。此反应的氧化剂是( )
2CrO3+3C2H5OH+3H2SO4=Cr2(SO4)3+3CH3CHO+6H2O
| A.H2SO4 | B.CrO3 | C.Cr2(SO4)3 | D.C2H5OH |
已知NH3和HCl都是能用来做喷泉实验的气体。若在同温同压下用等体积的一个烧瓶收集满NH3,另一个收集HCl气体未满,喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑溶质的扩散及静止时液面高度的影响)( )
| A.溶质的物质的量浓度相同、溶质的质量分数不同 |
| B.溶质的质量分数相同、溶质的物质的量浓度不同 |
| C.溶质的物质的量浓度和溶质的质量分数都不同 |
| D.溶质的物质的量浓度和溶质的质量分数都相同 |
3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g,则原硫酸的物质的量浓度为( )
| A.1 mol·L-1 | B.1.5 mol·L-1 |
| C.2 mol·L-1 | D.2.5 mol·L-1 |
有一瓶14%的KOH溶液,加热蒸发掉100 g水后,变为28%的KOH溶液80 mL,该80 mL溶液的物质的量浓度为( )
| A.5 mol/L | B.6 mol/L |
| C.6.25 mol/L | D.6.75 mol/L |
V LFe2(SO4)3溶液中含有a g SO42-,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为( )
A.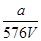 mol·L-1 mol·L-1 |
B.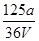 mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 |
D.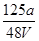 mol·L-1 mol·L-1 |