下列离子方程式书写正确的是
| A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性: 2H+ + SO42- + Ba2+ + 2OHOHOHOH- = BaSO4↓+ 2H2O |
| B.将标准状况下112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中: 2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 6Cl- + 2Br2 |
C.用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| D.向澄清石灰水中加入过量的碳酸氢钠溶液: Ca2+ + OHOHOHOH- + HCO3-= CaCO3↓ + H2O |
下列对有关物质性质的分析正确的是( )
| A.Na久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3 |
| B.在高温下用氢气还原MgCl2可制取金属镁 |
| C.实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性:CH3COOH>H2CO3 |
| D.N2的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
下列离子方程式书写正确的是( )
| A.用醋酸溶液除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.碘水中通入足量的SO2气体:I2+SO2+2H2O=2I-+SO42—+4H+ |
| C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42—+Ba2++OH-=BaSO4↓+H2O |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42—+3Cl-+H2O+4H+ |
下列物质的转化在给定条件下能实现的是( )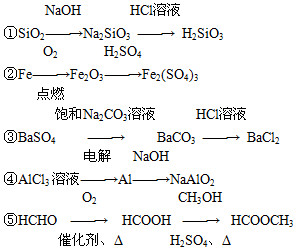
| A.①④⑤ | B.②③④ | C.②④⑤ | D.①③⑤ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.无色溶液:K+、Na+、Cu2+、SO42— |
| B.c(OH-)=10-13mol· L-1的溶液:Al3+、NO3—、I-、Cl- |
| C.水电离产生的c(H+)=10-13mol·L-1的溶液:Na+、Cl-、NO3—、SO42— |
| D.0.1 mol·L-1 FeSO4溶液:K+、NH4+、MnO4—、ClO- |
若用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A.1 mol BrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA |
| B.锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4 L,锌失去电子数为2NA |
| C.常温常压下,20 g D2O含有的原子总数为3NA |
| D.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数小于2NA |