把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为
| A.70% | B.52.4% | C.47.6% | D.30% |
随着卤素原子半径的增大,下列递变规律正确的是
| A.单质的熔、沸点逐渐降低 | B.气态氢化物稳定性逐渐增强 |
| C.卤素离子的还原性逐渐增强 | D.单质氧化性逐渐增强 |
根据元素在周期表中的位置判断,下列元素中原子半径最小的是
| A.氧 | B.氟 | C.碳 | D.氮 |
月球土壤中含有较丰富的3 2He,在地球上氦元素主要以4 2He的形式存在,下列说法正确的是
| A.3 2He代表原子核内有2个质子和3个中子的氦原子 |
| B.3 2He和4 2He互为同位素 |
| C.3 2He和4 2He分别含有1个和2个质子 |
| D.3 2He的最外层电子数为1,所以3 2He具有较强的金属性 |
已知:Fe2O3(s) + 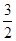 C(s) =
C(s) = 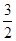 CO2(g) + 2 Fe(s)ΔΗ="+234.1" kJ·mol-1
CO2(g) + 2 Fe(s)ΔΗ="+234.1" kJ·mol-1
C(s) + O2(g) = CO2(g)ΔΗ="-393.5" kJ·mol-1
则2 Fe(s)+ 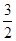 O2(g) = Fe2O3(s) 的ΔΗ是:
O2(g) = Fe2O3(s) 的ΔΗ是:
| A.-169.4kJ·mol-1 | B.-627.6 kJ·mol-1 |
| C.-744.7 kJ·mol-1 | D.-824.4 kJ·mol-1 |
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+ 的核外电子层结构相同。下列化合物中同时存在离子键和共价键的是:
| A.Z2Y | B.Z2Y2 | C.X2Y2 | D.ZYX |