工业上利用天然气(主要成分是CH4)与H2O进行高温重整制备合成气(CO+H2),CO和H2在一定条件下能制备甲醛、甲醚等多种有机物。已知CH4、H2和CO的燃烧热(△H)分别为-890.3 kJ·mol-1、-285.8 kJ·mol-1和-283.0 kJ·mol-1;18.0 g水蒸气液化时的能量变化为44.0 kJ。 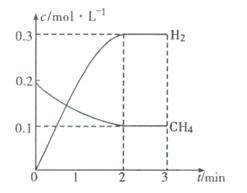
(1)写出甲烷与水蒸气在高温下反应制合成气的热化学方程式 。
(2)在一定条件下,向体积固定为2 L的密闭容器中充人0.40mol CH4(g)和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化的曲线如图所示。3 min时改变条件,反应进行到4 min时,体系中各物质的物质的量如下表所示:
| t/min |
n(CH4)/mol |
n(H2O)/mol |
n(CO)/mol |
n(H2)/mo1 |
| 4 |
0.18 |
0.38 |
0.22 |
0.66 |
则3~4min之间,平衡向 (填“正”或“逆”)反应方向移动,3min时改变的条件是 。
(3)已知温度、压强和碳水比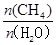 对该反应的影响如图所示。
对该反应的影响如图所示。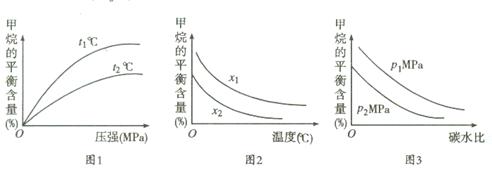
①图1中,两条曲线所示温度的关系:t1 t2(填“>”、“<”或“=”,下同)
②图2中,两条曲线所示碳水比的关系:x1 x2
③图3中,两条曲线所示压强的关系:p1 p2
(4)以天然气(假设杂质不参与反应)为原料的燃料电池示意图如图所示。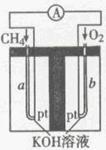
①放电时,正极的电极反应式为
②假设装置中盛装100.0 mL 3.0mol·L-1KOH溶液,放电时参与反应的氧气在标准状况下体积为8 960 mL。放电完毕后,电解质溶液中各离子浓度的大小关系为 。
甲、乙、丙是前18号元素形成的常见单质,A、B、C、D是前18号元素形成的不同化合物,甲、乙、丙和A、B、C、D有如下图所示的转化关系,丙是生命活动须臾不可缺少的气态单质,请回答下列问题:
(1)若甲为金属单质,A常温下为气体,则A的化学式为,写出反应①的化学方程式:;
标出反应②电子转移的方向和数目:
。
(2)若甲为非金属单质,A常温下为液态,则A的电子式为, C的化学式为,指出B的一种用途,写出反应②的离子方程式:。
(1)物质X是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
① 若X为氧化物,X的化学式是____________。
② 若X为单质,X用于焊接钢轨反应的化学方程式是_________________________。
③ 若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
X与稀硫酸反应的离子方程式是 ;
X与足量稀氢氧化钠溶液反应的离子方程式是。
(2)在宇航器中,可以不断的将座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,以除去A。反应的化学方程式是。
科学家设计出新的航天飞船内的空气更新系统。其中一步是A和氢气在200℃~250℃时,镍催化剂作用下,生成甲烷和另一种物质。该反应的化学方程式是________。
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+ 离子半径逐渐减小;化合物XN常温下为气体,据此回答: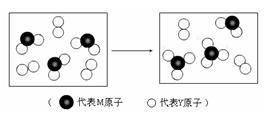
(1)写出Z与N形成化合物的电子式。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:。
(3)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:
。
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)  CH3OH(g)。根据题意完成下列各题:
CH3OH(g)。根据题意完成下列各题: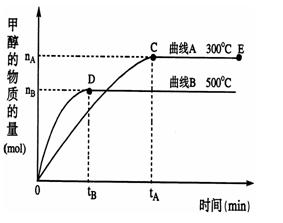
(1) 判断该反应达到平衡状态的标志是。(填字母)
a.CO和CH3OH浓度相等
b.CO百分含量保持不变
c.容器中气体的压强不变
d.CH3OH的生成速率与CO的消耗速率相等
e.容器中混合气体的密度保持不变
(2) 欲提高CO的转化率,下列措施可行的是
。(填字母)
a.向装置中再充入N2b.向装置中再充入H2
c .改变反应的催化剂 d.升高温度
.改变反应的催化剂 d.升高温度
(3) 反应达到平衡时,平衡常数表达式K=,升高温度,K值(填“增大”、“减小”或“不变”)。
(4) 在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(5) 在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(1)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g) H = -190 kJ·mol-1
H = -190 kJ·mol-1
该热化学反应方程式的意义是 ____________________________________。
(2) 处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知: CO (g)+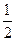 O2 (g) = CO2 (g)
O2 (g) = CO2 (g) H = -283.0 kJ·mol-1
H = -283.0 kJ·mol-1
S (g)+ O2 (g) = SO2 (g) H = -296.0 kJ·mol-1
H = -296.0 kJ·mol-1
此反应的热化学方程式是__________________________________________________。