(8分)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。请回答下列问题:
(1)已知: ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热____(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的气化热为44 kJ/mol,则表示氢气燃烧热的热化学方程式为______________________________。
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃)
该反应为_________反应(填“放热”或“吸热”);在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为____________________。
以苯酚为原料合成  的路线如下所示。请按要求作答
的路线如下所示。请按要求作答
(1)写出鉴别苯酚与A这2种有机物的有关反应方程式,并用必要的文字说明:
。
(2)写出以下物质的结构简式:
B,F。
(3)写出反应④的化学反应方程式:
④,
(4)反应⑤可以得到E,同时可能得到的副产物的结构简式为。
根据下列所给信息推断物质的组成或结构:
⑴已知化学式为C5H9Cl的某分子的所有碳原子和氯原子一定都在同一平面上,写出该分子的结构简式:。
⑵下面左图表示维生素A的分子结构: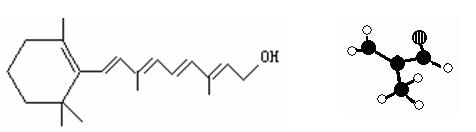
维生素A的分子式;维A属于。
A.酚类 B.不饱和有机物 C.链状化合物 D.芳香族化合物 E.醇类
⑶北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如上右图所示(图中球与球之间的连线代表化学键,如单键、双键等)该产品的键线式为,其核磁共振氢谱有个特征峰。
⑷某有机化合物仅由碳、氢、氧三种元素组成,其相对分子质量小于150,若已知其中氧的质量分数为50%,则分子中碳原子的个数最多为个。
现有四种有机物:①乙醇②苯酚③溴乙烷④乙烯,其中:
⑴能2步氧化生成乙酸的是。(填写序号,下同)。
⑵能发生消去反应生成烯烃的是。
⑶一定条件下能跟氢氧化钠溶液反应的是。
⑷在一定条件下能发生聚合反应的是。
某同学用10mol·L—1的浓盐酸配制250mL 1 mol·L—1的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸mL。
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
等。
(3)取所配制的稀盐酸100mL与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为多少克?(写出计算过程)
(4)设反应后溶液的体积仍为100mL,则反应后溶液中H+物质的量浓度是多少?(写出计算过程)
(1)下列反应中都有水参加:
| A.Cl2+ H2O +Na2SO3="=" 2HCl + Na2SO4 |
| B.3NO2 + H2O ="=" 2HNO3 + NO↑ |
| C.NaH +H2O ="=" NaOH + H2↑ |
| D.2H2O 电解2H2↑+ O2↑ |
其中,水只是氧化剂的是,水既不是氧化剂又不是还原剂的是,(各1分)
(2)在3BrF3+5H2O=9HF+HBrO3+O2↑+Br2反应中,若有5.4gH2O被氧化,
则被还原的BrF3共mol,其中被水还原的BrF3是mol。(各2分)