常温,下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1的溶液中: I-、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN- |
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是()
| 选项 |
操作及现象 |
溶液 |
| A |
向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色 |
含有Fe2+溶液 |
| B |
向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体 |
含有CO32-溶液 |
| C |
通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 |
可能为Ca(ClO)2溶液 |
| D |
通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊。 |
可能为Ca(OH)2溶液 |
某校活动小组为探究金属腐蚀的相关原理,设计了如下图a所示装置,图a的铁棒末段分别连上一块Zn片和Cu片,并静置于含有K3Fe(CN)6及酚酞的混合凝胶上。一段时间后发现凝胶的某些区域(如下图b示)发生了变化,已知Fe2+可用K3Fe(CN)6来检验(呈蓝色)。则下列说法不正确的是()

| A.甲区呈现红色 | B.乙区产生Zn2+ |
| C.丙区发生的电极反应式:Cu-2e-= Cu2+ | D.丁区呈现蓝色 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A.36gH2O和22.4LCO2中H和O,C和O之间的共价键均是4×6.02×1023 |
| B.0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 |
| C.常温常压下,4.6 g NO2气体含有0.1×6.02×1023个NO2分子 |
| D.0.1 mol的甲基(—CH3)和羟基(—OH)所含电子数均为0.9×6.02×1023 |
常温常压下,现有浓度为0.100 mol/L的六种溶液:①HCl,②H2SO4,③CH3COOH,④CH3COONa ⑤NaOH,⑥Na2CO3由水电离出的C(H+)大小关系正确的是()
| A.⑥>④>③>①=⑤>② | B.①=②>③>⑥>④>⑤ |
| C.②>①>③>④>⑥>⑤ | D.④>⑥>③>①=⑤>② |
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
反应一:Ni(粗,s)+4CO(g)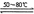 Ni(CO)4(g) ΔH < 0
Ni(CO)4(g) ΔH < 0
反应二:Ni(CO)4(g)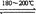 Ni(纯,s)+4CO(g) ΔH > 0下列说法错误的是()
Ni(纯,s)+4CO(g) ΔH > 0下列说法错误的是()
| A.对于反应一,适当增大压强,有利于Ni(CO)4的生成 |
| B.对反应二,在180—200℃,温度越高,Ni(CO)4(g)的转化率越高 |
| C.升高温度,反应一的反应速率减小,反应二的速率增大 |
| D.提纯过程中,CO气体可循环使用 |