氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2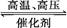 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式: 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS=-198.2 J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、Cu Cl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验。
Cl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀 。
。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。
由上述现象推断:该混合物中一定含有;一定不含有;可能 含有。
含有。
已知在标况下的四种气体①6.72L CH4 ②3.01×1023个HCl分子 ③13.6克H2S
④0.2molNH3用相应的序号填写下列空白:
(1)体积最大的是;(2)密度最大的是 ;
;
(3)质量最小的是;(4)含氢原子数最多的是。
气体化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10mLA气体能分解生成15mLO2和10mLF2(同温同压下),则A的化学式是,推断的依据是和。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、萃取分液法 B、加热分解C、结晶法D、分液法E、蒸馏法F、过滤法
(1)分离饱和食盐水和沙子的混合物;
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3)分离水和苯的混合物;
(4)分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶。
在VmLFe2(SO4)3溶液中含Fe3+ m g,取该溶液V/4mL,加水稀释至4VmL,则此稀溶液中SO42—的物质的量浓度为。