氢元素有1H、D、T三种原子,对于分别由它们形成的三种单质:
(1)在标准状况下,三种单质的密度之比是 。
(2)1 mol各种单质中,它们的质子数之比是 。
(3)1 g各种单质中它们的中子数之比是 。
(4)在标准状况下,1 L它们的单质中,它们的电子数之比是 。
请按要求完成下列各项填空:
(1)AlCl3的水溶液呈(填“酸”、“中”或“碱”)性,常温时的pH7(填“>”、“<”或“=”),原因是(用离子方程式表示):;实验室在配制 AlCl3溶液时,常将 AlCl3固体先溶于浓盐酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”或“抑制”)其水解。将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是(填化学式)。
(2)在纯碱溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是___________________________________________,其原因是(以离子方程式和简要的文字说明):
__________________________________________________________________________。
高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO(g)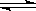 Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26
Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26
(1)写出该反应的平衡常数表达式:_______________________________。
(2)温度升高,化学平衡移动后达到新的平衡,平衡常数K值_________(填“增大”、“减小”或“不变”)。
(3)1100℃时,测得高炉中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,在这种情况下,该反应__________(填“已”或“没有” )处于化学平衡状态,此时化学反应速率V正 ______ V逆。(填“大于”、“小于”或“等于” )。
可用于分离或提纯物质的方法有:①过滤 ②蒸馏 ③加热分液(填序号)
(1)除去石灰水中悬浮的CaCO3颗粒
(2)除去NaCl晶体中混有的碘单质
(3)分离石油中各不同沸点范围的成分
(4)分离水和苯的混合物
(5)分离CCl4(沸点76.75℃)和甲苯(沸点110.6℃)____________。
2001年11月20日,解放日报报道:南太平洋岛国“图瓦卢被迫全国移民 “到新西兰。该国前总理佩鲁曾声称“图瓦卢是温室效应的第一个受害者”。目前该国正面临生存环境的严重恶化的局面。该国岛屿近20年来已被海水侵蚀的千疮百孔,岛上的淡水日益减少;海水的大量侵入使土壤盐碱化,粮食和蔬菜无法正常生长。图瓦卢陆地最高处仅海拔4.5m,由于海平面日渐升高,据估计这些岛屿将于50年内被海水淹没,请根据以上材料分析:
(1)图瓦卢是由多个珊瑚礁形成的岛国,由于大气中二氧化碳气体含量的剧增,大量珊瑚礁(主要成分是碳酸钙)被海水侵蚀,其原因是(用方程式表示)
(2)为了控制温室效应,各国科学家提出了不少方法和设想。有人根据液态二氧化碳气体的密度大于海水密度的事实,设想将二氧化碳液化后送入伸海海底。以减少二氧化碳气体的浓度。为使二氧化碳液化,可采用的方法是()
A、减压、升温 B、增压、升温 C、减压、降温 D、增压、降温
(3)科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有利于人类的物质。如将二氧化碳和氢气1:4的的物质的量比混合,通入反应器。在适当的条件下反应可获得一种重要的新能源。请完成以下化学方程式
 CO2+ 4H2() +2H2O
CO2+ 4H2() +2H2O
若将二氧化碳和氢气1:3的的物质的量比混合,在一定条件下生成某重要的化工原料和水,该化工原料可能是 ()
A、烷烃 B、烯烃 C、炔烃 D、芳香烃
煤是一种常用的燃料,由于煤燃烧产生的废气含有SO2、NO2和NO等多种有害气体和烟尘会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放
(1)将煤直接进行燃烧,造成环境污染的主要方面之一是形成硝酸型酸雨
①写出有关物质转化为硝酸的化学方程式
②以下是对硝酸型酸雨的若干项评价,其中正确的是
a:杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b:对电线,铁轨,桥梁,房屋等均会造成严重损害
c:导致臭氧层空洞
d:硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥。
(2)对煤用石灰石进行脱硫处理,过程中发生的方程式为:
(3)脱硫后,在废气中含有的不良气体是,它对环境的负面影响是。
(4)检验脱硫后废气中是否含有SO2的简单方法是。