[化学——选修2化学与技术]工业上常产生大量的废气、废水、废渣、废热,如果处理不好,随意排放,会造成污染,而如果科学回收,可变废为宝。
(1)一座大型硫酸厂同时又是一座能源工厂,硫酸厂生产过程中的余热若能充分回收利用,不仅不需要外界供应能源,而且还可以向外界输出大量的热能。硫酸厂产生余热的主要设备有________。
(2)硫酸厂产生的大量烧渣(硫铁矿煅烧后的灰渣)的用途是________(写一种即可);写出电解精炼铜阳极泥的一种用途________。
(3)工业制硫酸的尾气中含有的少量SO2,可先用氨水吸收,再用稀硫酸处理。
①该反应的化学方程式为_________;
②这样处理的优点是____________________。
(4)干熄焦技术是将炼焦炉推出的约1 000℃的赤热焦炭,在熄焦室中被其逆流的冷惰性气体(主要成分是氮气,温度在170~190℃)熄灭,被加热到700~800℃的惰性气体经除尘后进入余热锅炉,产生的过热蒸气送往汽轮发电机发电。干熄1 t焦炭可产生500 kg过热蒸气,可折合成46 kg标准煤。举出两例采用逆流原理的化工设备或化学仪器________、________。
(5)下图表示石灰-石膏法吸收SO2的工艺流程,写出反应的化学方程式 。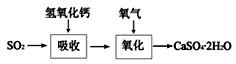
下列反应中氯元素全部被氧化的是____________,全部被还原的是____________,部分被氧化的是____________,既被氧化又被还原的是____________。
A.4HCl+MnO2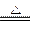 MnCl2+Cl2↑+H2O MnCl2+Cl2↑+H2O |
B.2NaCl 2Na+Cl2↑ 2Na+Cl2↑ |
| C.2KClO3====2KCl+3O2↑ | D.Cl2+H2O====HCl+HClO |
图所示的关系。
试回答下列问题:
(1)G的化学式为:。
(2)写出下列反应的化学方程式
①,
②。
(3)X在医药上用作解酸剂,与盐酸作用时,生成B的物质
的量与消耗盐酸的物质的量之比为3:8,则X的化学
式为:。
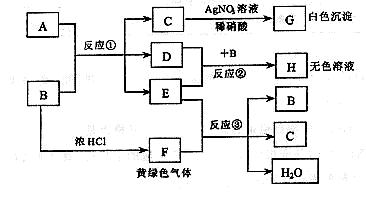
请回答:
(1) 依次写出A、B 中溶质的化学式:A_______ B________
(2) 依次写出反应①和②的离子方程式(H 中含有某+5价元素含氧酸根离子)
______________________________ ; ___________________________
(3) 写出反应③的化学方程式___________________________________

(1) ③号元素位于周期表第____周期第_____族,其单质的一种同素异形体能导电,该同素异形体的名称叫________
⑵④号元素形成的气态氢化物的电子式为__________,属于_____分子(填极性或非极性)
⑶⑥、⑦两种元素形成的最高价氧化物对应的水化物之间相互反应的离子方程式为_____________________________
⑷⑨号元素的原子结构示意图为_______________________。⑨与⑤两种元素形成的一种化合物是污染大气的主要有害物质之一,它对环境的危害主要是:
Ⅰ. 加入3mol SO2和2mol O2发生反应,达到平衡时放出的热量为 ____________
Ⅱ. 保持同一反应温度,在相同容器中,将起始物质的量改为 a mol SO2、 b mol O2 、c mol SO3 (g) ,欲使平衡时SO3的体积分数为2/9。
⑴达到平衡时,Ⅰ和Ⅱ放出的热量 ______(填序号)
A.—定相等 B.前者一定小 C. 前者大于或等于后者
(2) a、b、c必须满足的关系是(一个用a、c表示,另一个用b、c表示)________________