某溶液中加入铝粉有氢气产生,该溶液中肯定可以大量共存的离子组是 ( )
A.Na+、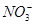 、Cl-、 、Cl-、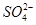 |
B.Na+、K+、Ba2+、 |
C.Fe3+、H+、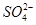 、Cl- 、Cl- |
D.Na+、K+、Cl-、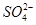 |
下列实验操作正确的是( )
| A.用结晶法除去硝酸钾中混有的少量氯化钠 |
| B.用湿润的pH试纸测定Na2CO3溶液的pH |
| C.Zn和烯硫酸反应时,为了使制取氢气的速度加快,可向稀硫酸中加入一定量的水 |
| D.在氢氧化铁胶体中加入过量的盐酸最终会产生沉淀 |
下列实验操作中:①过滤;②蒸发;③溶解;④取液体试剂;⑤取固体试剂。一定要用到玻璃棒的是( )
| A.①②③ | B.④⑤ |
| C.①④ | D.①③⑤ |
利用重结晶法得到KNO3晶体时,如用较多量的蒸馏水洗涤将会( )
| A.提高收率和纯度 |
| B.降低收率和纯度 |
| C.提高收率和降低纯度 |
| D.降低收率和提高纯度 |
在实验室中进行粗食盐水的精制时,为了除去粗食盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗食盐溶于水,然后进行下列五项操作。其中正确的操作顺序是(双选)( )
①过滤 ②加过量的NaOH溶液 ③加适量盐酸
④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ |
| C.②⑤④①③ | D.⑤②④①③ |
欲使CuSO4·5H2O、NH4Cl和SiO2的混合物分离,其必要的实验操作为( )
| A.升华 溶解 过滤 蒸发 |
| B.溶解 过滤 萃取 分液 |
| C.加热 溶解 过滤 结晶 |
| D.溶解 过滤 分馏 结晶 |