铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物。某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验。
(1)取磁性氧化铁按图中甲装置进行铝热反应,现象很壮观。取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种结果的原因,除了可能混有没反应的磁性氧化铁外,还有一个原因是 。
(2)为了克服图中甲的缺陷,改用图中乙装置进行铝热反应,主要步骤如下:
①在一个广口容器中放进一定量的干燥细沙;
②将一定量的铁砂和铝粉混合物装在纸漏斗中并埋入细沙里;
③将一定量的镁粉和氯酸钾混合物放在铝热剂上;
④再放上引火剂;引火反应,冷却;⑤取出反应后的铁块(如图丙)
请写出铝热反应的化学方程式:
取少许反应生成的铁块溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。实验中干燥细沙的主要作用是 。
(3)测定图中乙反应所得的铁块纯度,流程如下图所示。几种氢氧化物开始沉淀和沉淀完全时的pH参考19题。
①试剂A应选择 ,试剂B应选择 。
| A.稀盐酸 | B.氧化铁 | C.H2O2溶液 | D.氨水 E.MgCO3固体 |
②操作Ⅰ的名称为 。操作Ⅱ的名称为 。固体M完全转化为固体N的标志是 。
③已知常温下Fe(OH)3的KSP=4.0×10-38,求反应Ⅲ后溶液中c(Fe3+)= mol/L
④若最终红色粉末质量为14.14g,则该铁块的纯度是 。如果直接洗涤、烘干和称量固体M的质量,计算铁块的纯度,则计算结果会 (填“偏大”“偏小”或“无影响“)。原因是 。
实验室制配0.4mol/L的NaCl溶液100 mL,有以下仪器:①烧杯 ②100 mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦药匙
(1)配制时,还缺少的仪器是____________。
(2)应称取的NaCl固体的质量是____________克。
(3)实验两次用到玻璃棒,其作用分别是:
_____________、____________。
⑷配制时,一般过得程是:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥洗涤 ⑦摇匀 ⑧定容 ⑨摇匀。其中最后一次摇匀的方法是_____________(a、左右旋转摇匀B、上下颠到反复摇匀)
“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验。因其具有许多优点,已被广泛应用于化学实验中。下列三个实验均为“套管实验”,请观察、分析,回答下列问题: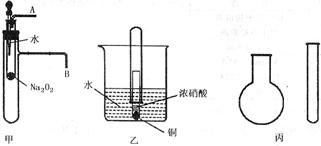
实验一:图甲是对课本有关Na2O2某性质的两个实验的改进。
⑴将胶头滴管中的水滴入小试管,然后,在导管口A、B处分别进行适当操作,再根据所观察现象可得到的两个结论是___________________,_________________。
⑵写出甲中反应的离子方程式_________________________________。
实验二:图乙是对铜和浓硝酸反应实验的改进。
⑶写出铜和浓硝酸反应的离子方程式为_________________________________。
⑷反应开始后,能观察到的现象是__________________________________,随后气体颜色逐渐变浅;大试管中液面上升。
⑸与普通演示实验相比,此实验除操作方便之外,还有_____________等优点。
实验三、现有下列药品:A.氯化铵固体,B.氢 氧化钠固体,C.浓氨水,D.浓硫酸,E.碳酸氢铵。采用“套管法”,只用一支试管(药匙等辅助用品略,不加热),选择合适的药品就可在圆底烧瓶中集满喷泉实验用的氨气(如图丙)。
氧化钠固体,C.浓氨水,D.浓硫酸,E.碳酸氢铵。采用“套管法”,只用一支试管(药匙等辅助用品略,不加热),选择合适的药品就可在圆底烧瓶中集满喷泉实验用的氨气(如图丙)。
⑹此实验制备氨气选用的最合适药品是__________(填序号)。
Fe3O4一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
▲提出假设:假设1. 黑色粉末是CuO;假设2. 黑色粉末是Fe3O4;
假设3. ______________________________。
▲设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
⑴若假设1成立,则实验现象是________________。
⑵若所得溶液显血红色,则假设_________成立。
⑶为进一步探究,继续向所得溶液加入足量铁粉,若产生_______的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
⑷为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生__________现象,则假设2成立;若产生______________现象,则假设3成立。
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯 ;②固定铁圈位置 ;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热。其正确的操作顺序为。
(2)如何运用最简方法 检验溶液中SO42-是否除尽?。如果还有,应该如何除去SO42-离子?。
检验溶液中SO42-是否除尽?。如果还有,应该如何除去SO42-离子?。
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的
 。
。
(4)将经过操作(3)后的溶液过滤。请问这一操作能除掉哪些杂质? 。
。
右图为实验室某浓盐酸试剂瓶标签上的有关数据,
试根据标签上的有关数据回答下列问题:
⑴该浓盐酸中HCl的物质的量浓度为 mol·L-1。 ⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是。
| A.溶液中HCl的物质的量 | B.溶液的浓度 | C.溶液中Cl-的数目 | D.溶液的密度 |