C、N、O、Na、Al、S、Cl是常见的元素
(1)C元素位于元素周期表的位置 ;C元素的一种同位素可以测定文物年代,这种同位素的符号为 。
(2)用“>”、“<”或“=”填空
| 离子半径 |
酸性 |
还原性 |
得电子能力 |
| N3- Al3+ |
H2SO4 HClO4 |
O2- S2- |
35Cl 37Cl |
(3)黑火药爆炸时发生反应的化学方程式为:S+2KNO3 +3C==K2S +3CO2↑+N2↑反应生成物中,属于非电解质的是_______(写结构式);其中熔点最高的物质的电子式是_________。
(4)在(3)中化学反应方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为_________,能证明其递变规律的事实是( )(填字母)
A.氧化物对应水化物的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.氢化物的稳定性
芳香烃X是一种重要的有机化工原料,其摩尔质量为92g·mol一1,某课题小组以它为原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。已知A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
已知: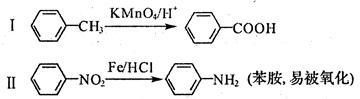
回答下列问题:
(1)对于阿司匹林,下列说法正确的是_______
| A.是乙酸的同系物 |
| B.能发生酯化反应 |
| C.1 mol阿司匹林最多能消耗2mol NaOH |
| D.不能发生加成反应 |
(2)H的结构简式是_________,F→G的反应类型是_______。
(3)写出C→D的化学方程式_______。
( 4)写出符合下列条件的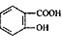 的同分异构体的结构简式_______。(写出2种)
的同分异构体的结构简式_______。(写出2种)
①属于芳香族化合物,且能发生银镜反应;
②核磁共振氢谱图中峰面积之比为1 :2:2:1
③分子中有2个羟基
(5)以A为原料可合成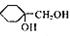 ,请设计合成路线,要求不超过4步(无机试剂任选)。
,请设计合成路线,要求不超过4步(无机试剂任选)。
注:合成路线的书写格式参照如下示例流程图:
可降解聚合物G可由芳香烃A通过如下途径制备,质谱法测定A相对分子质量为102。
已知①B为高分子化合物,D的化学式为C8H10O2
②
③碳碳双键的碳上连有羟基的有机物不稳定
(1)对于高分子G的说法不正确的是()
A.1mol G最多能与2n mol NaOH反应
B.一定条件下能发生取代与加成反应
C.碱性条件下充分降解,F为其中一种产物
D.(C9H8O3)n既是高分子G的化学式也是其链节的化学式
(2)A、X的化学式分别为________________ ,
(3)写出C→D的化学方程式 。
(4)写出B的结构简式
(5)同时符合下列条件F的稳定同分异构 体共 种,写出其中一种结构简式
①遇FeCl3不显紫色,除苯环外不含其它环状结构;
②苯环上有三种不同化学环境的氢原子;
③不能发生银镜反应。
(6)以苯和乙烯为原料可合成D,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下实例流程图:
CH3CHO  CH3COOH
CH3COOH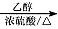 CH3COOCH2CH3
CH3COOCH2CH3
药物普仑司特对预防和治疗中耳炎、银屑病等均有良好疗效。在普仑司特的合成中需要用到关键中间体M(1﹣溴﹣4﹣苯丁烷)。中间体M的合成路线如下:
已知:
回答下列问题:
(1)D中的官能团为 :反应④属于 反应(填反应类型);
B的结构简式为 。
(2)写出一种满足下列条件的A的同分异构体的结构简式: 。
A.能发生银镜反应和水解反应: B.不存在顺反异构体
(3)利用溴代烃E (含溴质量分数为66.1%)为起始原料也可制得中间体M:
则E的结构简式为
F→M的化学方程式为 。
(4)C6H5MgBr与化合物G在一定条件下直接反应可制得M。①用系统命名法给化合物G命名: ;②写出加热条件下G在足量NaOH醇溶液中反应的化学方程式: 。
合成肉桂酸异戊酯G(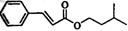 )的路线如下:
)的路线如下:
友情提示:
①B和C含有相同的官能团且C在标准状况下的气体密度为1.964g/L;
② 。
。
回答下列问题:
(1)A的结构简式为 ,D中含有的官能团的名称是 ;
(2)下列物质在一定条件下能与F反应的是 (填标号);
A.溴水 B.酸性KMnO4溶液 C.乙酸 D.新制氢氧化铜的悬浊液
(3)B和C反应生成D的化学方程式为 。
(4)E和F反应生成G的化学方程式为 ,反应类型为 。(各2分)
(5)A的同分异构体中含有苯环的共有 种(不考虑立体异构且包括A),其中与氯化铁不能发生显色反应且核磁共振氢谱有四组峰,峰面积之比为3:2:2:1的为______ (写结构简式)。(各2分)
有增长碳链是有机合成中非常重要的反应。例如:
反应①
用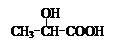 通过以下路线可合成(Ⅱ):
通过以下路线可合成(Ⅱ):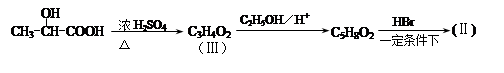
(1)(Ⅰ)的分子式为 ;1mol该物质完全燃烧需要消耗 mol O2.。
(2)(Ⅱ)与足量的热NaOH溶液反应的化学方程式为 。
(Ⅲ)的结构简式为 ;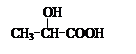 在生成(Ⅲ)时,还能得到另一种副产物C6H8O4,该反应的化学方程式为 ,该反应的反应类型是 。
在生成(Ⅲ)时,还能得到另一种副产物C6H8O4,该反应的化学方程式为 ,该反应的反应类型是 。
(4)对二氯苯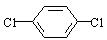 也能与有机物(Ⅰ) (过量)发生类似反应①的系列反应,其生成有机物的结构简式为 。
也能与有机物(Ⅰ) (过量)发生类似反应①的系列反应,其生成有机物的结构简式为 。