硫、氯及其化合物有广泛的用途。
(1)“氯氧化法”是指在碱性条件下用Cl2将废水中的CN-氧化成无毒的物质。CN-被氧化后的产物为 (填化学式)。
(2)“氯胺(NH2Cl)消毒法“是在用液氯处理自来水的同时通入少量的氨气,发生反应: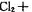
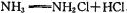 ,生成 的NH2Cl能部分水解生成强氧化性的物质,起消毒杀菌的作用。氨氯能用于消毒杀菌的原因是 (用化学方程式表示)。
,生成 的NH2Cl能部分水解生成强氧化性的物质,起消毒杀菌的作用。氨氯能用于消毒杀菌的原因是 (用化学方程式表示)。
(3)如图所示装置和药品可用来制备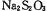 。
。
①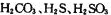 三种酸的酸性由强到弱的顺序位 。
三种酸的酸性由强到弱的顺序位 。
②配平广口瓶中生成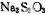 反应的化学方程式:
反应的化学方程式:
根据下图所示,推断物质X的化学式。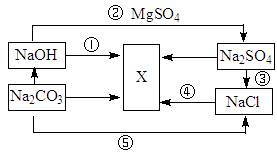
X的化学式
某混合物由NaCl、MgCl2两种物质组成,其中Na和Mg两种元素的质量比为23∶12。求
⑴NaCl与MgCl2的物质的量之比。
⑵氯离子总量为8mol时,Mg2+的物质的量是 。
。
8.4g N2与9.6g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是,x值为。
同温同压下,某瓶充满氧气时质量为116g,充满二氧化碳时,质量为122g,充满气体A时质量为114g,A的摩尔质量为________。
同温同压下,同体积的氨气(NH3)和硫化氢气体(H2S)的质量比为;同质量的氨气和硫化氢气体的体积比为其中含有的氢原子个数比为;若二者氢原子数相 等,它们的体积比为。
等,它们的体积比为。