某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-):Na+、NH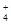 、SO
、SO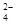 、CO
、CO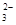 、NO
、NO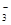 。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
| A.该溶液中可能含有Na+ |
B.该溶液中肯定含有NH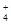 、SO 、SO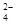 、CO 、CO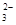 、NO 、NO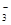 |
C.该溶液中一定不含NO |
| D.该溶液中一定含有Na+,且c(Na+)≥0.1 mol·L-1 |
已知Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g)ΔH<0,则下列叙述不正确的是
| A.该反应中旧化学键断裂需要吸收能量,新化学键形成需要放出能量,所以反应前后物质具有的总能量不变 |
| B.上述热化学方程式中的ΔH的值与实验测定中反应物的用量无关 |
| C.该反应的化学能可以转化为其他形式的能 |
| D.反应物的总能量高于生成物的总能量 |
右图中的曲线是表示其他条件一定时,2NO(g)+O2(g) 2NO2(g) ΔH<0反应中NO2的百分含量与温度的关系曲线,图中标有a 、b 、c 、d四点,其中表示未达到平衡状态,且v正>v逆的点是
2NO2(g) ΔH<0反应中NO2的百分含量与温度的关系曲线,图中标有a 、b 、c 、d四点,其中表示未达到平衡状态,且v正>v逆的点是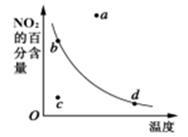
| A.a点 | B.b点 | C.c点 | D.d点 |
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ•mol-1、-1411.0kJ•mol-1和-1366.8kJ•mol-1,( C2H4、C2H5OH(1)充分燃烧后的产物为CO2和H2O),则由C2H4(g)和H2O(l)反应生成C2H5OH(1)的△H为
| A.-44.2kJ•mol-1 | B.+44.2kJ•mol-1 | C.-330kJ•mol-1 | D.+330kJ•mol-1 |
已知某化学反应的平衡常数表达式为K=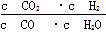 ,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是
,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是
| t℃ |
700 |
800 |
830 |
1 000 |
1 200 |
| K |
1.67 |
1.11 |
1.00 |
0.60 |
0.38 |
A.该反应的化学方程式是CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol,该反应达到平衡状态
D.某温度下,如果平衡浓度符合下列关系式: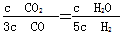 ,判断此时的温度是1 000℃
,判断此时的温度是1 000℃
工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。设在容积为1.0 L的密闭容器中充入0.5 mol N2(g)和1.0mol H2(g),某温度下反应达到平衡时容器内压强为原来的2/3,则该反应的平衡常数
2NH3(g)。设在容积为1.0 L的密闭容器中充入0.5 mol N2(g)和1.0mol H2(g),某温度下反应达到平衡时容器内压强为原来的2/3,则该反应的平衡常数
| A.4 | B.16 | C.32 | D.64 |