常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示: 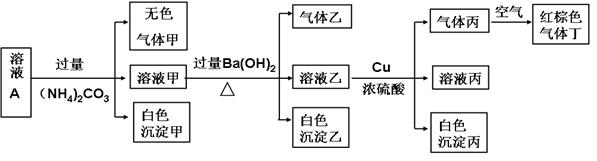
下列有关说法正确的是 ( )
| A.沉淀乙一定有BaCO3,可能有BaSO4 |
| B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L |
| C.该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子 |
| D.生成的甲、乙、丙气体均为无色的易溶于水气体 |
2006年5月24日夜间,一辆油罐车在贝宁经济首都科托努以北500多千米的波尔加起火,事故现场发现了23具被烧焦的尸体,造成至少35人死亡,60多人受伤。这辆由科托努开往贝宁北部的油罐车因发生故障停在路边,附近的居民用管子偷吸油罐车里的汽油时,其中一人携带的油灯引燃了油罐车。近年来,我国许多城市禁止汽车使用含铅汽油,其主要原因是()
| A.提高汽油燃烧效率 | B.降低汽油成本 |
| C.避免铅污染大气 | D.防止铅与汽油反应 |
下列有水参加的反应,其中是氧化还原反应且水既不是氧化剂又不是还原剂的是()
| A.钠跟水 | B.氧化钠跟水 | C.过氧化钠跟水 | D.电解水 |
向紫色石蕊试液中加入过量的Na2O2粉末振荡,可观察到的现象为( )
| A.溶液仍为紫色 |
| B.溶液最终变蓝色 |
| C.最终溶液褪色,而无其他现象 |
| D.溶液中有气泡产生,溶液最终变为无色 |